Методы решения расчетных задач по химии с использованием химической реакции в процессе приготовления раствора
В наиболее сложных задачах, в дополнение к вычислениям по теме «растворы», предполагается расчет по уравнению реакции. Приведен пример решения задачи на приготовление растворов ацетальдегида, а также дана задача на приготовление раствора формалина.
Задача 1.
В результате гидратации ацетилена объемом 67,2 л (н.у.) можно получить водный раствор ацетальдегида с массовой долей 15%. Масса полученного раствора равна ... г. (запишите число с точностью до целых).
Дано:
объем ацетилена (н.у.): V(С2Н2) = 67,2 л;
массовая доля ацетальдегида в растворе:  (Н3С-НС=О) = 15%.
(Н3С-НС=О) = 15%.
Найти: массу раствора: mр-ра = ?
Решение:
М(Н–НС=О) = 30 г/моль.
1. Записываем уравнение реакции и рассчитываем по нему массу образовавшегося ацетальдегида:
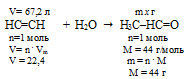
Составляем пропорцию:
67,2 л HC=CH дает х г H3C–HC=O (по условию);
22,4 л НС=СН дает 44 г H3C–HC=O (по уравнению);
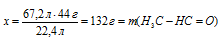
2. Находим массу 15%-ного раствора, содержащего 132 г ацетальдегида:
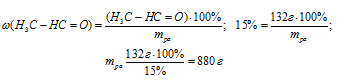
Ответ: mр-ра = 880 г.
Кроме реакции гидратации ацетилена, в задачах, аналогичных последней, использовались реакции взаимодействия оксидов щелочных и щелочноземельных металлов с водой.
Рассмотрим условие еще одной задачи, встречающейся в некоторых вариантах последних лет. Ее текст вызывает некоторое непонимание среди тестируемых и требует пояснений.
Задача 2.
Объем формальдегида, который потребуется для получения 1 л раствора (р = 1,11 г/мл) с массовой долей формалина 40% равен ... л. В задаче имеется в виду, что путем растворения формальдегида получается 1 л раствора формалина (р = 1,11 г/мл) с массовой долей формальдегида 40%1.
Дано:
массовая доля формальдегида в растворе: (Н–НС=О) = 40%;
(Н–НС=О) = 40%;
плотность раствора формальдегида: рр-ра = 1,11 г/л.
Найти: Объем формальдегида: V(Н–НС=О) = ?
Решение:
1. Находим массу 1 л раствора формалина:
mр-ра = Vр-ра . рр-ра = 1000 мл . 1,11 г/л = 1110 г.
2. Находим массу формальдегида, которая требуется для получения 1 л раствора (р = 1,11 г/мл) с массовой долей формалина 40%, с применением соотношения для определения массовой доли:
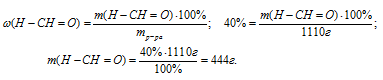
3. Находим объем формальдегида, с учетом , что формальдегид в данных условиях является газом, получим:
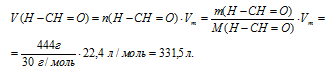
Ответ: V(Н–НС=О) = 331,5 л.
Комментарии:
1Непонимание вызвала фраза: «1л раствора (р = 1,11 г/мл) с массовой долей формалина». Дело в том, что формалин — это уже 40% раствор формальдегида в воде. Некоторые учащиеся решили, что разбавлению подлежит формалин и требуется получить новый раствор, в котором массовая доля исходного раствора (формалина) будет 40%.
Источник:
ЕГЭ. Химия. Расчетные задачи в тестах ЕГЭ. Части А, В, С / Д.Н. Турчен. — М.: Издательство «Экзамен», 2009. — 399 [1]с. (Серия «ЕГЭ. 100 баллов»). I8ВN 978-5-377-02482-8.

