Решение пяти типовых задач "В9" по химии на тему "Растворы"
Задача 1.
Массовая доля растворенных солей в некотором образце морской воды составляет 3,3%. Определите массу солей, содержащихся в 100,0 л такой воды (р = 1,12 г/мл). Ответ: ... г (запишите число с точностью до целых).
Дано:
объем раствора морской воды: Vр-ра — 100,0 л;
массовая доля солей :  (НNO3) = 3,3%;
(НNO3) = 3,3%;
плотность раствора: pр-ра = 1,12 г/мл.
Найти: массу солей: mсолей = ?
Решение :
В первую очередь необходимо от объема раствора перейти к его массе, используя плотность. При этом следует учесть, что объем указан в литрах, а плотность в г/мл. Переведем значение
объема в единицы измерения, соответствующие плотности.
Vр-ра = 100 л = 100000 мл;
mр-ра = Vр-ра . рр-ра =
= 100000 . 1,12 = 112000г.
Далее используем соотношение для определения массовой доли.
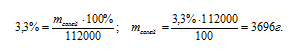
Ответ: mсолей = 3696 г.
Задача 2.
Масса серной кислоты, содержащейся в 2 л ее водного 30%-ного раствора (р = 1,22 г/мл), равна ... г (запишите число с точностью до целых).
Дано:
объем раствора: Vр-ра — 2 л;
массовая доля раствора серной кислоты: (H2SO4) = 30%
(H2SO4) = 30%
плотность раствора: pр-ра = 1,22 г/мл.
Найти: массу серной кислоты: m(H2SO4) = ?
Решение :
В первую очередь необходимо от объема раствора перейти к его массе, используя плотность. При этом следует учесть, что объем указан в литрах, а плотность в г/мл. Переведем значение объема в единицы измерения, соответствующие плотности.
Vр-ра = 2 л = 2000 мл;
mр-ра = Vр-ра . рр-ра = 2000 . 1,22 = 2440г.
Далее используем соотношение для определения массовой доли.
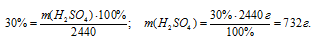
Ответ: m(H2SO4) = 732 г.
Задача 3.
Масса сахарозы, содержащейся в 1 л ее водного 50%-ного раствора (р = 1,23 г/мл) равна….. г (запишите число с точностью до целых).
Дано:
объем раствора: Vр-ра — 1 л;
массовая доля раствора сахарозы:  (С12Н22О11) = 50%;
(С12Н22О11) = 50%;
плотность раствора: pр-ра = 1,23 г/мл.
Найти: массу сахарозы: m(С12Н22О11) = ?
Решение :
В первую очередь необходимо от объема раствора перейти к его массе, используя плотность. При этом следует честь, что объем указан в литрах, а плотность в г/мл. Переведем значение объема в единицы измерения, соответствующие плотности.
Vр-ра = 1 л = 1000 мл
mр-ра = Vр-ра . рр-ра = 1000 . 1,23 = 1230 г.
Далее используем соотношение для определения массовой доли.
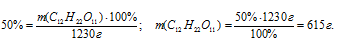
Ответ: m(12Н22О11) = 615 г.
Задача 4.
Масса этанола, содержащегося в 2 л его 56%-ного водного раствора (р = 0,900 г/мл) равна ... г (запишите число с точностью до целых).
Дано:
объем раствора: Vр-ра — 2 л;
массовая доля раствора этанола: (С2Н6О) = 56%;
(С2Н6О) = 56%;
плотность раствора: pр-ра = 0,900 г/мл.
Найти: массу сахарозы: m(С2Н6О)) = ?
Решение :
В первую очередь необходимо от объема раствора перейти к его массе, используя плотность. При этом следует учесть, что объем указан в литрах, а плотность в г/мл. Переведем значение
объема в единицы измерения, соответствующие плотности.
Vр-ра = 2 л = 2000 мл;
mр-ра = Vр-ра . рр-ра = 2000 . 0,900 = 1800 г.
Далее используем соотношение для определения массовой доли.
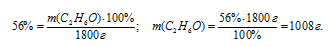
Ответ: m(С2Н6О) = 1008 г.
Задача 5.
Массовая доля соляной кислоты, полученной растворением 33,6 л (н.у.) хлороводорода в 1,5 л воды, равна ... % (запишите число с точностью до сотых).
Дано:
объем раствора: Vр-ра = 1,5 л;
объем хлороводорода: V(HCl) = 33,6 л.
Найти: массовую долю раствора хлороводорода: (HCl) = ?
(HCl) = ?
Решение:
М(HCl) = 36,5 г/моль.
m(H2O) = 1500 мл . 1г/мл = 1500 г
В первую очередь необходимо найти массу газообразного хлороводорода, растворенного в 1,5 л воды.
m(HCl) = n(HCl) . M(HCl) = V(HCl)/Vm . M(HCl) =
= 33,6 л/22,4л/моль . 36,5 г/моль = 54,75 г.
2. Находим массу раствора:
mр-ра = m(H2O) + m(HCl) =
= 1500 г + 54, 75 г = 1554,75 г.
3. Далее используем соотношение для определения массовой доли.
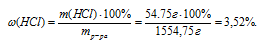
Ответ:  (HCl) = 3,52%.
(HCl) = 3,52%.

