"Химия. 11 класс". О.С. Габриелян (гдз)
Сравнение свойств органических и неорганических соединений
Опыт 1. Образование солей взаимодействием органических и неорганических оснований и кислот, опыты с ними.
Выполнение работы:
Смешали 2 капли анилина и немного воды, получили эмульсию анилина. В другую пробирку налили немного CuSO4 и по каплям при встряхивании добавили NаОН, получили голубой осадок Cu(OH)2.
В обе пробирки по каплям добавили концентрированную НСI. Наблюдаем растворение эмульсии и осадка.
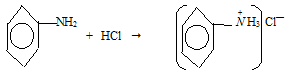
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
К образовавшимся растворам добавили по каплям концентрированный раствор NаОН, осадки вновь выпали.
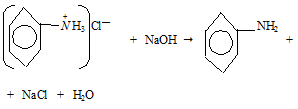
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
Вывод: органические и неорганические основания и соли проявляют схожие свойства.
Опыт 2. Получение сложных эфиров взаимодействием органических и неорганических кислот со спиртами.
а). В пробирку налили немного изоамилового спирта и концентрированной уксусной кислоты и добавили чуть-чуть концентрированной серной кислоты. Смесь перемешали и нагрели на водяной бане. Наблюдаем пожелтение жидкости. Смесь остудили, эфир собрался на поверхности, ощущаем запах грушевой эссенции.
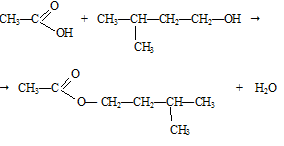
б) В фарфоровую чашку поместили несколько кристаллов борной кислоты и прибавили немного этилового спирта. Смесь перемешали и поднесли к ней зажженную лучинку. Образовавшееся вещество сгорело зеленым пламенем.
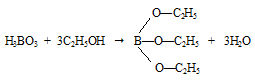
2В(ОС2Н5)3 + 18О2 → В2О3 + 12СО2 + 15Н2О
Вывод: органические и неорганические кислоты проявляют аналогичные химические свойства.
Опыт 3. Амфотерность гидроксида цинка и аминоуксусной кислоты.
а) В две пробирки налили немного раствора нитрата цинка и добавили к нему по каплям раствор NaOН, до выпадения осадка. Затем в одну пробирку налили раствор НСI, а в другую раствор NaOН. осадки растворились в обеих пробирках.
Zn(NO3)2 + 2NaOH ↔ Zn(OH)2↓ + 2NaNO3;
Zn(OH)2 + 2HCl ↔ ZnCl2 + 2H2O;
Zn(OH)2 + 2NaOH ↔ Na2[Zn(OH)4].
б) В пробирку налили немного раствора карбоната натрия и присылали в пробирку немного глицина. Наблюдаем выделение пузырьков газа СО2. Глицин проявляет свои кислотные свойства. Поместили в пробирку несколько кристаллов глицина и смочили их концентрированной соляной кислотой. Пробирку нагрели. Наблюдаем растворение глицина. Поместили каплю полученного раствора на предметное стекло. При охлаждении наблюдаем образование кристаллов, отличных по форме от кристаллов глицина.
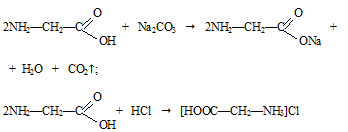
Вывод:
амфотерные соединения существуют и в органической и в неорганической химии и проявляют схожие свойства.
Опыт 4. Сравнение свойств солей.
Выполнение работы:
а) В 2 пробирки налили понемногу растворов нитрата и ацетата свинца. Затем в каждую пробирку прилили раствор КI. Наблюдаем выделение осадка РbI2.
Pb(NO3)2 + 2KI ↔ PbI2↓ + 2KNO3;
(CH3COO)2Pb 2KI ↔ PbI2↓ + 2CH3COOK.
б) В две пробирки налили понемногу растворов сульфата меди(I) и соли анилина. Добавили в обе пробирки концентрированный раствор NаОН. Наблюдаем выпадение осадков:
CuSO4 + 2NaOH ↔ Cu(OH)2↓ + Na2SO4
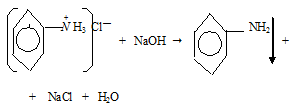
Вывод:
и органические, и неорганические соли проявляют схожие свойства.

