Как правильно определить формулу кристаллогидрата соли
Задача 1017.
При прокаливании 30 г кристаллогидрата сульфата кальция выделяется 6,28 г воды. Какова формула кристаллогидрата?
Решение:
Mr(CaSO4) = 136 a. e.;
Mr(H2O) = 18 a. e.
Находим массу CaSO4, получим:
M(CaSO4) = 30 – 6,28 = 23,78 г.
Обозначим количество молекул CaSO4 в кристаллогидрате через «х», а количество молекул воды – через «у», получим: (CaSO4)х . (Н2О)у.
Определим соотношение х : у, получим:
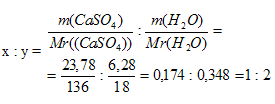
Значит, формула кристаллогидрата имеет вид: (CaSO4)х . (Н2О)у или CaSO4 . Н2О.
Ответ: CaSO4 . Н2О.
Задача 1018.
При растворении в кислоте 5,00 г СаО, содержащего примесь СаСО3, выделилось 140 мл газа, измеренного при нормальных условиях. Сколько процентов СаСО3 (по массе) содержалось в исходной навеске?
Решение:
М(СаСО3) = 136г/моль
Уравнение реакции:
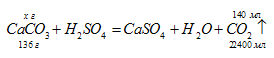
Рассчитаем массу СаСО3 в навеске из пропорции:
136 : 22400 = х : 140;
х = (136 . 140)/22400 = 0,85 г.
Находим массовую долю СаСО3:
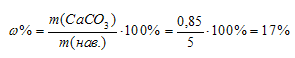
Ответ: 17%.

