Алгоритмы решения адач на получение раствора путем смешивания двух исходных растворов
Смешение двух исходных растворов
3адача 49.
В каком соотношении (по массе) необходимо смешать 5%-ный и 9%-ный (масс.) растворы КОН в воде для получения 6% -ного раствора.
Дано:
массовая доля КОН в 1 исходном р-ре:  (КОН)в1 исх. р-ре = 5%;
(КОН)в1 исх. р-ре = 5%;
массовая доля КОН во 2 исходном р-ре: (КОН)во 2 исх. р-ре = 9%;
(КОН)во 2 исх. р-ре = 9%;
массовая доля КОН в конечном р-ре:  (КОН)кон. р-ре = 6%/
(КОН)кон. р-ре = 6%/
Найти:
соотношение исходных растворов: m1 исх.р-ра : m2 исх. р-ра.
Решение:
Отобразим условие задачи в виде рисунка:

Схематично алгоритм решения можно представить так
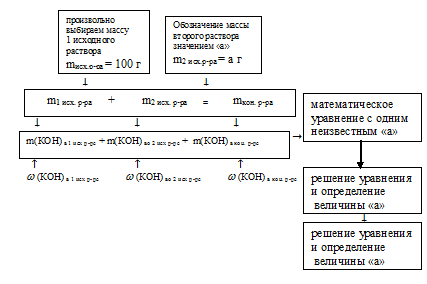
1. Обозначим массу второго исходного 9%-ного раствора КОН величиной «а»: т2 исх р-ра = а г.
Тогда масса конечного 6% -ного раствора получится:
mкон. р-ра = m1 исх. р-ра + m2 исх. р-ра = (100 + а) г.
2. Теперь определяем массу чистого КОН в каждом из трех растворов:
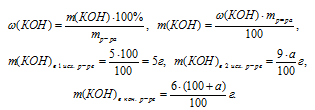
3. Масса чистого КОН в конечном растворе складывается из сумм масс КОН в исходных двух растворах. Составим математическое уравнение
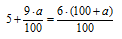
Решая его, получаем: а = 33,3.
4. Величиной «а» мы обозначали массу второго 9%-ного раствора, следовательно:
m2 исх. р-ра = 33,3 г
Массу же первого исходного раствора мы приняли равной 100 г. Находим соотношение масс исходных растворов:
m1 исх. р-ра : m2 исх. р-ра = 100 : 33,3 = 3 : 1.
Ответ: исходные растворы нужно смешать в соотношении m(5% -ного р-ра) : т(9% ного р-ра) = 3:1.
Определение массы соли в приготовленном растворе
Задача 50.
Определите массу соли NаС1, которую необходимо добавить к 900 г 2%-ного раствора NаС1 в воде, чтобы получить 4% -ный раствор.
Дано:
масса исходного раствора: mисх. p-ра = 900 г;
массовая доля NаС1 исходном растворе:  (NаС1)в исх р-ре = 2%;
(NаС1)в исх р-ре = 2%;
массовая доля NаС1 в конечном растворе:  (NаС1)в кон. р-ре = 4%/
(NаС1)в кон. р-ре = 4%/
Найти:
массу добавленной соли: m(NаС1)до6авл = ?
Решение:
Отобразим условие задачи в виде рисунка:
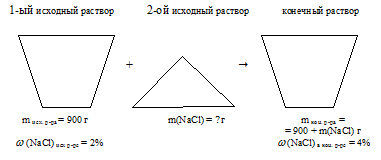
Схематично алгоритм решения можно представить так:
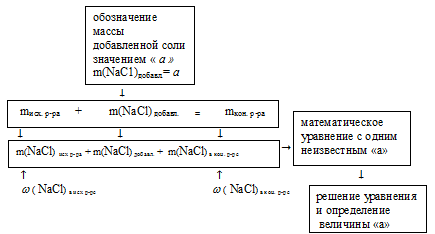
1. Искомой величиной является масса чистой соли NаС1. Обозначим ее величиной «а» : m(NаС1) = а г.
Тогда масса полученного раствора будет:
mкон. р-ра = mисх. р-ра + m(NаС1)до6авл = (900 + а) г.
2. Определим массу чистого NаС1 в исходном и полученном растворах.
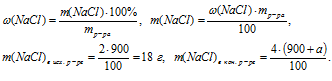
3. Масса чистого NаСl в полученном растворе складывается из суммы масс NаСl в исходном растворе и массы добавленной соли:
m(NаСl)в кон. р-ре = m(NаСl)в исх р-ре + m(NаСl)добавл.
Подставляем полученные выше величины:
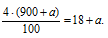
Решая это уравнение, получаем: а = 18,75.
Величиной «а» мы обозначали массу добавленной соли, следовательно:
m(NаСl)до6авл = 18,75 г.
Ответ: необходимо добавить 18,75 г NаСl.

