Определение массовой доли каждого вещества в растворе
Общая формула определения массовой доли имеет вид:
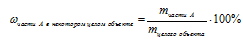
Для случая растворов формула определения массовой доли вещества конкретизируется в вид:
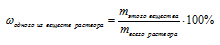
Задача 1.
Определить массовую долю каждого вещества в растворе, образованном из 15 г чистой уксусной кислоты и 235 г воды.
Дано:
масса воды: m(Н2О) = 235 г;
масса уксусной кислоты: m(СН3СООН) = 15 г.
Найти:
массовую долю воды;
массовую долю уксусной кислоты.
Решение:
Схематично алгоритм решения можно представить следующим образом:
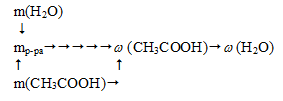
Масса всего раствора равна сумме масс уксусной кислоты и воды:
mр-ра = 15 + 235 = 250 г.
Подставляем данные в формулу для определения массовой доли:
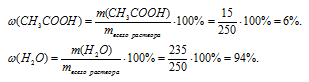
Сумма массовых долей всех веществ раствора всегда будет равна 100%. Поэтому для раствора состоящего из двух веществ достаточно указать массовую долю одного из них. Массовая доля второго вещества вычисляется по разнице:  2 = 100 –
2 = 100 –  1. Массовую долю воды в рассмотренной задаче мы могли вычислить тоже по разнице:
1. Массовую долю воды в рассмотренной задаче мы могли вычислить тоже по разнице:
 Н2О) = 100% –
Н2О) = 100% –  СН3СООН) =
СН3СООН) =
= 100% – 6% = 94%.
Ответ:  СН3СООН) = 6% ;
СН3СООН) = 6% ;  Н2О) = 94% .
Н2О) = 94% .
Задача 2.
В 600 г воды растворили 13 г КОН и 12 г NаОН. Определить массовую долю всех веществ в полученном растворе.
Дано:
масса воды: m(Н2О) = 600 г;
масса гидроксида калия: m(КОН) = 13 г;
масса гидроксида натрия: m(NаОН) = 12 г;
Найти:
массовую долю каждого из веществ в растворе.
Решение:
В этой задаче раствор состоит из трех веществ: Н2О, КОН и NaОН. Гидроксид калия химически не взаимодействует с гидроксидом натрия, поэтому новых веществ не образуется и ничего не расходуется.
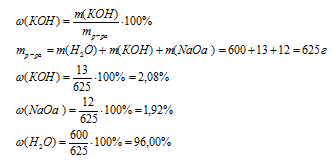
Массовую долю воды можно было найти и по разности:
 Н2О) = 100% –
Н2О) = 100% –  (КОН) –
(КОН) –  (NаОН) =
(NаОН) =
= 100 – 2,08 – 1,92 = 96% .
Ответ:  (КОН) - 2,08%;
(КОН) - 2,08%;  NаОН) = 1,92%;
NаОН) = 1,92%;  Н2О) = 96,00%.
Н2О) = 96,00%.
Задача 3.
При растворении 17 г МаОН в воде образовалось 36,8 мл раствора (р = 1,32 г/мл). Определите массовую долю NаОН в полученном растворе.
Дано:
масса гидроксида натрия: m(NаОН) = 17 г;
объем раствора: Vр-ра = 36,8 мл;
плотность раствора: рр-ра =1,32 г/мл.
Найти:  NaOH.
NaOH.
Решение:
Во всех задачах, в которых используется массовая доля необходимо от объема раствора переходить к массе. Переход от объемных единиц измерения к массовым осуществляется только через плотность по соотношению:
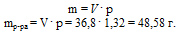
Находим массовую долю NаОН в растворе:
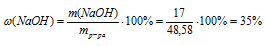
Ответ:  NаОН) = 35%.
NаОН) = 35%.

