Реакции диспропорционирования (самоокисления-самовосстановления)
Задание 370
Почему атомы большинства р-элементов способны к реакциям диспропорционирования (самоокисления-самовосстановления)? На основании электронных уравнений напишите уравнение реакции серы в концентрированном растворе щелочи. Один из продуктов содержит серу в степени окисления +4.
Решение:
Атомы р-элементов имеют конфигурацию внешнего электронного слоя ns2np(1-6). Большинство из них способны к диспропорционированию, потому что атомы многих из них содержат на внешнем электронном слое такое количество электронов, что могут их отдавать или же присоединять, т. е. одновременно уменьшать и увеличивать свою степень окисления. Например, сера содержит на внешнем электронном слое шесть электронов два s-электрона и четыре р-электрона. Благодаря наличию свободных d-орбиталей степень окисления серы меняется от -2 до +6. Сера может одновременно менять свою степень окисления от 0 до -2 и от 0 до +6.
Уравнение реакции серы в концентрированном растворе щелочи:
Уравнения электронного баланса:
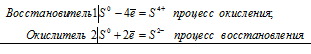
3S0 = S4+ + 2S2-
Молекулярное уравнение реакции:
3S+ 6NaOH = Na2SO3 + 2Na2S + 3H2O
Задание 371.
Почему сернистая кислота может проявлять как окислительные, так и восстановительные свойства? На основании электронных уравнений составьте уравнения реакций Н2SO3: а) с сероводородом; б) с хлором.
Решение:
Поскольку в Н2SO3 атом серы находится в своей промежуточной степени окисления +4, то возможны процессы восстановления и окисления, т. е. сера в сернистой кислоте может присоединять электроны, понижая свою степень окисления, а также отдавать электроны, повышая свою степень окисления. Например, легко протекает реакция H2SO3 с сероводородом и с хлором:
а) реакция сернистойкислоты с сероводороом
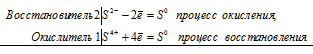
2S2- + S4+ = 3S0
Молекулярное уравнение реакции:
H2SO3+ 2H2S = 3S + 3H2O
б) реакция сернистой кислоты с хлором
Уравнения электронного баланса:
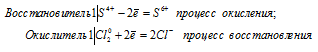
Cl20 + S4+ = S6+ + 2Cl-
Молекулярное уравнение реакции:
H2SO3+ Cl2 = SO3↑ + 2HCl
Задание 373
Почему азотистая кислота может проявлять как окислительные, так и восстановительные свойства? На основании электронных уравнений составьте уравнения реакций НNO2: а) с бромной водой; б) с HI.
Решение:
Поскольку в НNO2 азот находится в своей промежуточной степени окисления +3, то азотистая кислота в окислительно-восстановительных реакциях может быть как восстановителем, так и окислителем. Сильные окислители переводят NO2- в NO3-. Сильные восстановители обычно восстанавливают НNO2 до NO. Азотистая кислота способна также к реакциям самоокисления-самовосстановления, которых азот как уменьшает, так и увеличивает свою степень окисления.
Уравнения реакций НNO2 с бромной водой и с HI:
а) реакция азотистой кислоты НNO2 с бромной водой
Уравнения электронного баланса:
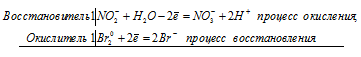
NО2- + Br20 + H2O = NО3- + 2Br- + 2H+
Молекулярное уравнение реакции:
НNO2 + Br2 + H2O = НNO3 + 2HBr
б) реакция НNO2 с HI:
Уравнения электронного баланса:
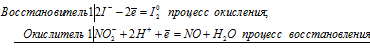
NО2- + 2I- +4H+ = NО + I20 + 2H2O
Молекулярное уравнение реакции:
2НNO2 + 2HI = I2 + 2NO + 2H2O
Задание 374
Почему диоксид азота способен к реакциям самоокисления-самовосстановления (диспропорционирования)? На основании электронных уравнений напишите уравнение реакции растворения NO2 в гидроксиде натрия.
Решение:
Поскольку в NO2 азот находится в своей промежуточной степени окисления +4, то диоксид азота может вступать в реакции самоокисления-самовосстановления, в которых атом азота одновременно уменьшает и увеличивает свою степень окисления.
Уравнение реакции растворения NO2 в гидроксиде натрия:
Уравнения электронного баланса:
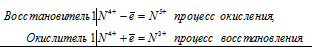
2N4+ = N5+ + N3+
Молекулярное уравнение реакции:
2NO2 + 2NaOH = NaNO2 + NaNO3
Задание 377
Почему фосфористая кислота способна к реакциям самоокисления - самовосстановления диспропорционирования)? На основании электронных уравнений составьте уравнение процесса разложения Н3РО3, учитывая, что при этом фосфор приобретает низшую и высшую степени окисления.
Решение:
Поскольку в молекуле Н3РО3 атом фосфора находится в своей промежуточной степени окисления +3, то фосфористая кислота диспропорционирует, т. е. атомы фосфора в реакции самоокисления-самовосстановления одновременно могут, как увеличивать свою степень окисления, так и уменьшать её. Так при нагревании Н3РО3 диспропорционирует с образованием Н3РО4 и РН3:
Уравнения электронного баланса:
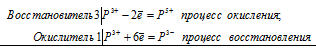
4Р3+ = Р5+ + Р3-
Молекулярное уравнение реакции:
4Н3РО3 = 3Н3РО4 + РН3↑

