Окислительно-восстановительные свойства азота и фосфора
Задание 369.
На основании электронных уравнений составьте уравнение реакции фосфора с азотной кислотой, учитывая, что фосфор приобретает высшую степень окисления, а азот - степень окисления +4.
Решение:
Уравнения электронного баланса:
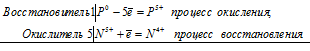
P0 + 5N5+ = P5+ + 5N4+
Молекулярное уравнение реакции:
Р + 5НNO3 = H3PO4 + 5NO2↑ + H2O
Задание 376
В каком газообразном соединении азот проявляет свою низшую степень окисления? Напишите уравнения реакций получения этого соединения: а) при взаимодействии хлорида аммония с гидроксидом кальция; б) разложением нитрида магния водой.
Решение:
Азот проявляет свою низшую степень окисления в газообразном соединении NH3. Степень окисления атома азота в аммиаке равна -3.
Уравнения реакции получения аммиака:
а) при взаимодействии хлорида аммония с гидроксидом кальция:
2NH4Cl + Ca(OH)2 ⇔ 2NH3↑+ CaCl2 + 2H2O
б) разложением нитрида магния водой:
Mg3N2 + 6H2O ⇔ 3Mg(OH)2↓ + 2NH3↑
Задание 378
В каком газообразном соединении фосфор проявляет свою низшую степень окисления? Напишите уравнения реакций: а) получения этого соединения при взаимодействии фосфида кальция с хлороводородной (соляной) кислотой; б) горения его в кислороде.
Решение:
В газообразном соединении РН3 (фосфин) атом фосфора проявляет свою низшую степень окисления -3.
Уравнения реакций:
а) получения РН3 при взаимодействии фосфида кальция с хлороводородной (соляной) кислотой:
Са3Р2 + 6HCl ⇔ 3CaCl2 + 2PH3↑;
б) горения фосфора в кислороде:
4Р + 5О2 = 2Р2О5 (или 4Р + 5О2 = Р4О10.
Задание 386
Какие реакции нужно провести, имея азот и воду, чтобы получить нитрат аммония? Составьте уравнения соответствующих реакций.
Решение:
Из воды можно получить кислород по реакции:
2Н2О 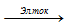 2Н2 + О2
2Н2 + О2
Затем из смеси азота, кислорода и воды можно получить нитрат аммония NH4NO3:
2N2 + O2 + 4H2 → 2NH4NO3
Можно из азота и воды получить смесь аммиака и азотистой кислоты, из которых в смеси с кислородом получить нитрат аммония:
2Н2О 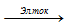 2Н2 + О2;
2Н2 + О2;
N2 + 2H2O → NH3 + HNO2;
2NH3 HNO2 + O2 → 2NH4NO3

