Составление уравнений ядерных реакций. Изотопы, изобары
Задание 26.
Изотоп никеля-57 образуется при бомбардировке частицами ядер атомов железа-54. Составьте уравнения ядерной реакции и напишите его в сокращенной форме.
Решение:
Изотоп 28-го элемента – никель-57 был получен бомбардировкой -частицами атомов железа-54. Превращение атомных ядер обуславливается их взаимодействием с элементарными частицами или друг с другом. Ядерные реакции связаны с изменением состава ядер атомов химических элементов. С помощью ядерных реакций можно из атомов одних эле-ментов получить атомы других. Превращение атомных ядер как при естественной, так и при искусственной радиоактивности записывают в виде уравнения ядерных реакций. При этом следует помнить, что суммы массовых чисел (цифры, стоящие у символа элемента вверху слева) и алгебраические суммы зарядов (цифры, стоящие у символа элемента внизу слева) частиц в левой и правой частях равенства должны быть равны. Данную ядерную реакцию выражают уравнением:
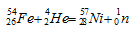
Часто применяют сокращённую форму записи ядерной реакции. Для данной реакции она будет иметь вид:
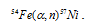
В скобках пишут бомбардирующую частицу, а через запятую – частицу, образующуюся при данном ядерном процессе. В сокращённых уравнениях частицы:
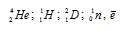
обозначают соответственно  , p, d, n, е.
, p, d, n, е.
Задание 28.
Что такое изотопы? Чем можно объяснить, что у большинства элементов периодической системы атомные массы выражаются дробным числом? Могут ли атомы разных элементов иметь одинаковую массу? Как называются подобные атомы?
Решение:
Атомы, обладающие одинаковым зарядом ядра (и, следовательно, тождественными химическими свойствами), но разным числом нейтронов (а значит, и разным массовым числом), называют изотопами (от греч. слов «изос» - одинаковый и «топос» - место). Установлено, что, как правило, каждый элемент представляет собой совокупность нескольких изотопов. Именно этим объясняются значительные отклонения атомных масс многих элементов от целочисленных величин. Так, природный хлор на 75,53% состоит из изотопа 35Cl и на 24,47% из изотопа 37Cl; в результате средняя атомная масса хлора равна 35,453.
В природе встречается и другое явление, заключающееся в том, что атомы разных элементов обладают одинаковой атомной массой, но разным зарядом ядер. Такие атомы называют изобарами. Например, изотоп калия 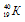 и изотоп кальция
и изотоп кальция 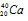 имеют одинаковые атомные массы (40), но разные заряды ядер Соответственно +19 и +20:
имеют одинаковые атомные массы (40), но разные заряды ядер Соответственно +19 и +20:
Задание 29.
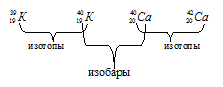
Изотоп кремния-30 образуется при бомбардировке  -частицами ядер атомов алюминия-27. Составьте уравнение этой ядерной реакции и напишите его в сокращенной форме.
-частицами ядер атомов алюминия-27. Составьте уравнение этой ядерной реакции и напишите его в сокращенной форме.
Решение:
Превращение атомных ядер обуславливается их взаимодействием с элементарными частицами или друг с другом. Ядерные реакции связаны с изменением состава ядер атомов химических элементов. С помощью ядерных реакций можно из атомов одних элементов получить атомы других. Превращение атомных ядер как при естественной, так и при искусственной радиоактивности записывают в виде уравнения ядерных реакций. При этом следует помнить, что суммы массовых чисел (цифры, стоящие у символа элемента вверху слева) и алгебраические суммы зарядов (цифры, стоящие у символа элемента внизу слева) частиц в левой и правой частях равенства должны быть равны. Данную ядерную реакцию выражают уравнением:
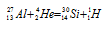
Часто применяют сокращённую форму записи ядерной реакции. Для данной реакции она будет иметь вид:
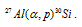
В скобках пишут бомбардирующую частицу, а через запятую – частицу, образующуюся при данном ядерном процессе. В сокращённых уравнениях частицы
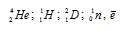
обозначают соответственно  , p, d, n, е.
, p, d, n, е.
Задание 31.
Изотоп углерода-11 образуется при бомбардировке протонами ядер атомов азота- 14. Составьте уравнение этой ядерной реакции и напишите его в сокращенной форме.
Решение:
Превращение атомных ядер обуславливается их взаимодействием с элементарными частицами или друг с другом. Ядерные реакции связаны с изменением состава ядер атомов химических элементов. С помощью ядерных реакций можно из атомов одних элементов получить атомы других. Превращение атомных ядер как при естественной, так и при искусственной радиоактивности записывают в виде уравнения ядерных реакций. При этом следует помнить, что суммы массовых чисел (цифры, стоящие у символа элемента вверху слева) и алгебраические суммы зарядов (цифры, стоящие у символа элемента внизу слева) частиц в левой и правой частях равенства должны быть равны. Данную ядерную реакцию выражают уравнением:
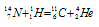
Часто применяют сокращённую форму записи ядерной реакции. Для данной реакции она будет иметь вид:
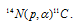
В скобках пишут бомбардирующую частицу, а через запятую – частицу, образующуюся при данном ядерном процессе. В сокращённых уравнениях частицы:
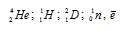
обозначают соответственно  , p, d, n, е.
, p, d, n, е.
Задание 328
Назовите три изотопа водорода. Укажите состав их ядер. Что такое тяжелая вода? Как она получается и каковы ее свойства?
Решение:
Для водорода известны три изотопа: - протий Н, - дейтерий D, - тритий Т. Протий и дейтерий встречаются в природе, тритий получен искусственно. Ядро протия состоит из одного протона, ядро дейтерия - из одного протона и одного нейтрона, а ядро трития – из одного протона и двух нейтронов.
Тяжёлая вода D2O – соединение дейтерия с кислородом. Тяжёлую воду получают путём электролиза природной воды. При электролизе воды разряд ионов Н+ происходит значительно быстрее, чем D+, поэтому в остатке после разложения электролизом большого количества воды концентрируется D2O.
Тяжёлая вода D2O по физико-химическим свойствам отличается от Н2О: tпл. = 3,82 0С, tкип. = 101,42 0С, рплот, равна 1,1050 г/см3 (20 0C). Заметно различаются энтальпии растворения солей в Н2O и D2O, константы диссоциации кислот и другие характеристики растворов.

