Приготовление раствора соли с заданной массовой долей из её кристаллогидрата
Задача 406.
Для приготовления 5%-ного (по массе) раствора MgSO4 взято 400 г MgSO4 . 7Н2О. Найти массу полученного раствора.
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением:
m(в-ва) =  . m(кристаллогидрата),
. m(кристаллогидрата),
где
 - массовая доля соли в кристаллогидрате, которую можно определить по формуле:
- массовая доля соли в кристаллогидрате, которую можно определить по формуле:
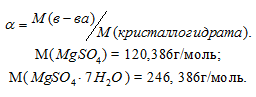
Тогда
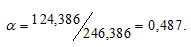
Масса MgSO4 в 400 г MgSO4 . 7Н2О будет равна:
m(MgSO4) =  . m(MgSO4 . 7Н2О) =
. m(MgSO4 . 7Н2О) =
= 0,487 . 400 = 195,443г.
Для расчета массы раствора используем формулу:
 ,
,
где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Отсюда
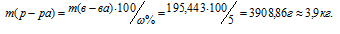
Ответ: 3,9 кг.
Задача 407.
Сколько молей MgSO4 . 7Н2О надо прибавить к 100 молям воды, чтобы получить 10%-ный (по массе) раствор MgSO4?
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением:
m(в-ва) =  . m(кристаллогидрата),
. m(кристаллогидрата),
где
 - массовая доля соли в кристаллогидрате, которую можно определить по формуле:
- массовая доля соли в кристаллогидрате, которую можно определить по формуле:
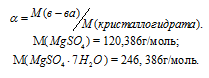
Тогда
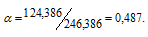
Для расчета массы кристаллогидрата используем формулу:
 ,
,
где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Обозначим массу кристаллогидрата MgSO4 . 7Н2О через х, а массу MgSO4 через  . y.
. y.
Тогда рассчитаем массовую долю MgSO4, подставив соответствующие значения в уравнение, получим:
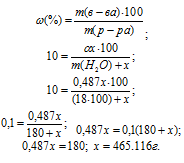
Для расчета количества кристаллогидрата используем формулу: 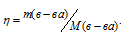
Отсюда
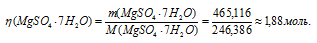
Ответ: 1,88 моль.
Задача 408.
Определить массовую долю CuSO4 в растворе, полученном при растворении 50 г медного купороса CuSO4 . 5H2O в 450 г воды.
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением: m(в-ва) =  . m(кристаллогидрата) , где
. m(кристаллогидрата) , где  - массовая доля соли в кристаллогидрате, которую можно определить по формуле:
- массовая доля соли в кристаллогидрате, которую можно определить по формуле:
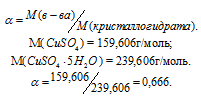
Тогда
Масса раствора равна:
m(CuSO4) =  . m(CuSO4 . 5H2O) =
. m(CuSO4 . 5H2O) =
= 0,666 . 50 - 33,3г.
Массовую долю CuSO4 находим из уравнения:
 ,
,
где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Отсюда
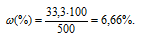
Ответ: 6,66%.
Задача 409.
В какой массе воды нужно растворить 25 г CuSO4 . 5H2O, чтобы получить 8%-ный (по массе) раствор CuSO4?Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением: m(в-ва) =  . m(кристаллогидрата), где
. m(кристаллогидрата), где  - массовая доля соли в кристаллогидрате, которую можно определить по формуле:
- массовая доля соли в кристаллогидрате, которую можно определить по формуле:
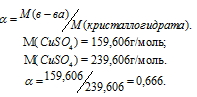
Тогда масса CuSO4, содержащаяся в 25 г медного купороса равна:
m(CuSO4) =  . m(CuSO4 . 5H2O) =
. m(CuSO4 . 5H2O) =
= 0,666 . 25 - 16,65г.
Массу полученного раствора находим из уравнения:
 ,
,
где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Отсюда масса раствора равна:
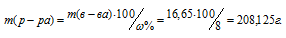
Тогда масса воды, которую необходимо прибавить к 25 г медного купороса, будет равна:
208,125 – 25 = 183,125г.
Ответ: 183,125 г.
Задача 410.
Сколько граммов Na2SO4 . 10H2O надо растворить в 800г воды, чтобы получить 10%-ный (по массе) раствор Na2SO4?
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением:
m(в-ва) =  . m(кристаллогидрата),
. m(кристаллогидрата),
где
 - массовая доля соли в кристаллогидрате, которую можно определить по формуле:
- массовая доля соли в кристаллогидрате, которую можно определить по формуле:
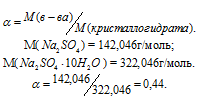
Для расчета массы кристаллогидрата используем формулу:
 ,
,
где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Обозначим массу кристаллогидрата Na2SO4 . 10H2O через х, а массу Na2SO4 через  . x, получим выражение:
. x, получим выражение:
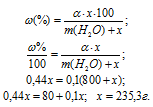
Ответ: 235,3 г.

