Как вычислить константу равновесия реакции
Задача 366.
В каком направлении сместится равновесие реакции А2(г) + В2(г) ⇔ 2АВ(г), если давление увеличить в 2 раза и одновременно повысить температуру на 10 градусов? Температурные коэффициенты скорости прямой и обратной реакций равны соответствен-но 2 и 3. Каков знак  этой реакции?
этой реакции?
Решение:
Поскольку реакция А2(г) + В2(г) ⇔ 2АВ(г) является простой гомогенной, то для неё можно записать выражение Закона Действия Масс (ЗДМ) прямой и обратной реакций:
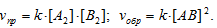
После увеличения давления в системе в 2 раза, соответственно, в 2 раза увеличится концентрация всех реагентов системы, имеем:
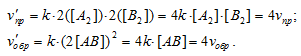
Таким образом, при увеличении давления в системе vпр = vобр, значит, равновесие не сместится.
Подставив данные задачи в выражение правила Вант-Гоффа, получим:
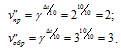
Таким образом, vпр < vобр, значит, равновесие системы сместится влево, в сторону реакции с меньшей скоростью.
Повышение температуры в системе, согласно правилу Ле Шателье, приводит к смещению равновесия системы в направлении реакции, сопровождающейся поглощением теплоты, т.е. влево, значит прямая реакция экзотермическая,  < 0.
< 0.
Ответ: влево,  < 0.
< 0.
Задача 367.
Пользуясь табличными данными, вычислить константы равновесия следующих реакций при 298 и при 1000 К:
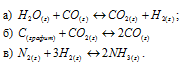
Изменениями  и
и  с температурой пренебречь.
с температурой пренебречь.
Решение:
По табличным данным стандартные значения  веществ, участвующих в реакции равны:
веществ, участвующих в реакции равны:
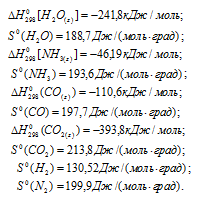
Стандартные значения 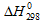 простых веществ равны нулю.
простых веществ равны нулю.
а) Находим стандартное значение  и
и  реакции Н2О(г) + СО(г) ⇔ СО2(г) + Н2(г):
реакции Н2О(г) + СО(г) ⇔ СО2(г) + Н2(г):
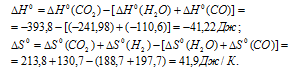
Находим значение энергии Гиббса реакции из уравнения  =
=  - T
- T , получим:
, получим:

Рассчитаем константу равновесия реакции при температуре 298 K, используя формулу:
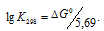
Тогда
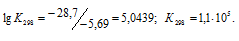
Константу равновесия реакции при температуре 1000 К, рассчитаем по формуле:
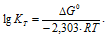
Тогда
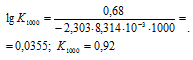
б) Находим стандартное значение  и
и  реакции C(графит) + СО2(г) ⇔ 2СО(г):
реакции C(графит) + СО2(г) ⇔ 2СО(г):
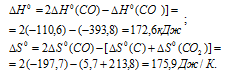
Находим значение энергии Гиббса реакции при температурах 298 К и 1000 К из уравнения  =
=  - T
- T , получим:
, получим:

Рассчитаем константу равновесия реакции при температуре 298 К, используя формулу:
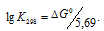
Тогда
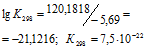
Константу равновесия реакции при температуре 1000 К, рассчитаем по формуле:
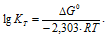
Тогда
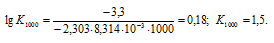
в) Находим стандартное значение  и
и  реакции N2(г) + 3H2(г) ⇔ 2NH3(г):
реакции N2(г) + 3H2(г) ⇔ 2NH3(г):
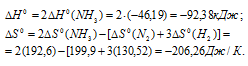
Находим значение энергии Гиббса реакции при температурах 298 К и 1000 К из уравнения  =
=  - T
- T , получим:
, получим:
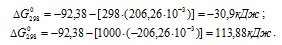
Рассчитаем константу равновесия реакции при температуре 298 К, используя формулу:
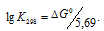
Тогда
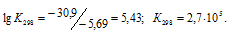
Константу равновесия реакции при температуре 1000 К, рассчитаем по формуле:
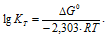
Тогда
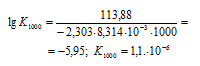
Ответ: а) 1,1 . 105, 0,92; б) 7,5 . 10-22, 1,5; в) 2,7 . 105, 1,1 . 10-6.
Задача 368.
Вычислить температуру, при которой константа равновесия реакции 2NO2(г) ⇔ N2O4(г) равна единице. Изменениями  и
и  с температурой пренебречь. В каком направлении сместится равновесие при температуре более низкой, чем найденная?
с температурой пренебречь. В каком направлении сместится равновесие при температуре более низкой, чем найденная?
Решение:
Уравнение реакции имеет вид: 2NO2(г) ⇔ N2O4(г).
Из уравнения 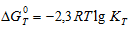 следует, что при KT = - 1 стандартная энергия Гиббса химической реакции равна нулю. Тогда из соотношения
следует, что при KT = - 1 стандартная энергия Гиббса химической реакции равна нулю. Тогда из соотношения 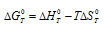 вытекает, что при
вытекает, что при 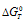 = 0, получим: 0 =
= 0, получим: 0 = 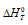 - T
- T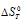 или
или 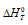 = T
= T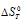 , откуда
, откуда
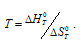
Согласно условию задачи можно пренебречь зависимостью  и
и  от температуры и для расчётов использовать стандартные значения энтальпии и энтропии. Стандартные значения
от температуры и для расчётов использовать стандартные значения энтальпии и энтропии. Стандартные значения 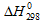 и
и  298 реагирующих веществ равны:
298 реагирующих веществ равны:
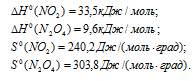
Находим  реакции, используя следствие из закона Гесса:
реакции, используя следствие из закона Гесса:
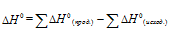
Тогда
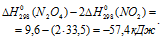
Теперь рассчитаем  реакции:
реакции:
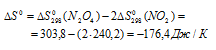
Отсюда
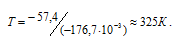
Ответ: 325 К.

