Теплота реакции. Следствия закона Гесса
Задача 298.
Вычислить 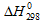 реакций:
реакций:
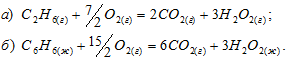
Решение:
По табличным данным стандартные энтальпии образования С2Н6(г), С6Н6(ж), Н2О(г), Н2О(ж) и СО2(г) соответственно равны -89,7, -241,8, 82,9, -241,8, -285,8 и -393,5 кДж/моль (стандартные энтальпии образования простых веществ принято считать равными нулю). Для расчета  реакций используем уравнение из следствия закона Гесса:
реакций используем уравнение из следствия закона Гесса:
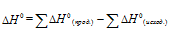
а) Находим стандартную энтальпию реакции:
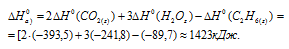
б) Находим стандартную энтальпию реакции:
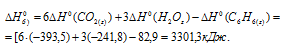
Ответ: а) 1423 кДж; б) 3301,3 кДж.
Задача 299.
Вычислить 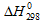 реакций:
реакций:
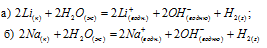
Стандартные энтальпии образования L1+(водн.), Na+(водн.) и OH-(водн.) принять соответственно равными -278,5, -239,7 и -228,9 кДж/моль.
Решение:
По условию задачи и по табличным данным стандартные энтальпии образования веществ равны:
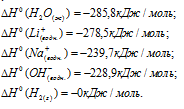
Для расчета  реакций используем уравнение из следствия закона Гесса:
реакций используем уравнение из следствия закона Гесса:
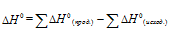
а) Находим стандартную энтальпию реакции:
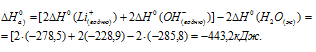
б) Находим стандартную энтальпию реакции:
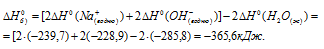
Ответ: а) -443,2кДж; б) -365,6 кДж.
Задача 300.
Вычислить значение 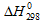 для протекающих в организме реакций превращения глюкозы:
для протекающих в организме реакций превращения глюкозы:
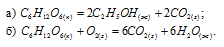
Какая из этих реакций поставляет организму больше энергии?
Решение:
По табличным данным стандартные энтальпии веществ, участвующих в реакциях равны (стандартные энтальпии простых веществ принято считать равными нулю):
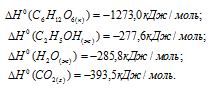
Для расчета  реакций используем уравнение из следствия закона Гесса:
реакций используем уравнение из следствия закона Гесса:
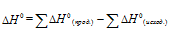
а) Находим стандартную энтальпию реакции:
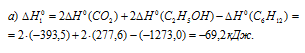
б) Находим стандартную энтальпию реакции:
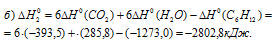
Реакция (б) поставляет организму больше энергии, чем реакция (а).
Ответ: а) -69,2 кДж; б) -2802,8 кДж.
Задача 301.
Зависит ли значение  реакции от присутствия в системе катализаторов? Ответ обосновать.
реакции от присутствия в системе катализаторов? Ответ обосновать.
Решение:
Катализаторы – это вещества, которые ускоряют процесс протекания химической реакции, но сами при этом в реакции не участвуют. Они ускоряют скорость как прямой, так и обратной реакции, но химическое равновесие системы не изменяют.
 - это изменение энтальпии или внутренней энергии системы в результате реакции.
- это изменение энтальпии или внутренней энергии системы в результате реакции.  зависит только от начального и конечного состояний, участвующих в реакции веществ и не зависит от промежуточных стадий процесса, в том числе и от скорости самой реакции ().
зависит только от начального и конечного состояний, участвующих в реакции веществ и не зависит от промежуточных стадий процесса, в том числе и от скорости самой реакции ().
 реакции определяется значениями стандартных энтальпий образования исходных веществ и продуктов реакции по уравнению из следствия закона Гесса:
реакции определяется значениями стандартных энтальпий образования исходных веществ и продуктов реакции по уравнению из следствия закона Гесса:
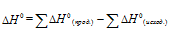
Задача 302.
Объяснить, почему процессы растворения веществ в воде могут самопроизвольно протекать не только с экзотермическим  < 0), но и с эндотермическим
< 0), но и с эндотермическим  > 0) эффектом.
> 0) эффектом.
Решение:
Процессы растворения веществ в воде могут самопроизвольно протекать как с выделением, так и с поглощением теплоты, потому что растворение веществ в воде является не только физическим, но и, одновременно, химическим процессом. Химический процесс может быть или эндотермическим  > 0) или экзотермическим
> 0) или экзотермическим  < 0) в зависимости от природы реагирующих веществ, в данном случае – от природы растворяемого вещества.
< 0) в зависимости от природы реагирующих веществ, в данном случае – от природы растворяемого вещества.

