Вычисление энтальпии образования вещества
Вычисление энтальпии образования озона из кислорода
Задача 6.
Исходя из энтальпий реакций окисления Аs2О3 кислородом и озоном:
Аs2О3 + О2 = Аs2О5; ∆Н°298х.р. = -271 кДж/моль;
3Аs2О3 + 2О3 = 3Аs2О5; ∆Н°298х.р. = -1096 кДж/моль, вычислите энтальпию образования озона из кислорода.
Решение:
Для решения задачи запишем оба уравнения реакций, умножим первое на три и вычтем из него второе.
3Аs2О3 + 3О2 = 3Аs2О5, 3∆Н°298х.р. =
= 3(-271кДж/моль);
3Аs2О3 + 2О3 = 3Аs2О5,∆Н°298х.р. = -1096кДж/моль.
(3Аs2О3 + 3О2) – (3Аs2О3 + 2О3) =
= (3Аs2О5 - 3Аs2О5), 3∆Н°298х.р.- ∆Н0298х.р.;
3О2 = 2О3, 3(-271 кДж/моль) - (-1096 кДж/моль) =
= -813 + 1096 = 283 кДж/моль.
Энтальпия образования озона из кислорода равна +283 кДж/моль.
А если учесть, что фактическое уравнение реакции образования озона из кислорода имеет вид:
1,5О2 = О3
Тогда
∆Н°(О3) = (283 кДж)/2 = 141,5 кДж.
1Ответ: ∆Н0(О3) = 141,5 кДж.
Вычисление энтальпии образования ацетилена по реакции его сгорания
Задача 7.
При сгорании 1 литра С2Н2 (О °С и 760 мм рт. ст.) выделяется 58,02 кДж тепла. Вычислить энтальпию образования ацетилена.
Решение:
В основе термохимических расчетов лежит закон Гесса (1840 г.): тепловой эффект реакции зависит только от природы и физического состояния исходных веществ и конечных продуктов, но не зависит от пути перехода.
В термохимических расчетах применяют чаще следствие из закона Гесса: тепловой эффект реакции (∆Hх.р.) равен сумме энтальпий образования ∆Hобр. продуктов реакции за вычетом суммы энтальпий образования исходных веществ с учетом стехиометрических коэффициентов:
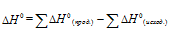
Запишем термохимическое уравнение реакции:
C2H2(г) + 5/2О2(г) = 2СО2(г) + Н2О(ж) + ∆Н°.
Из условия задачи вытекает, что при сгорании 1 л ацетилена выделяется 58,02 кДж. тепла. Находим ∆Н° при сгорании 1 моля ацетилена (С2Н2), получим:
58,02 . 22,4 = 1299,65кДж тепла,
т.е. ∆Н° = -1299,65 кДж.
Отсюда можно записать:
∆Н° = 2∆Н° (СО2) + ∆Н°(Н2О) – ∆°Н0(С2Н2) =
= –1299,65 кДж.
Тогда
∆Н°(С2Н2) = 2∆Н°(СО2) + ∆Н°(Н2О) – ∆Н° =
= 2∆Н0(СО2) + ∆Н0(Н2О) + 1299,65.
Пользуясь табличными данными:
∆Н°(СО2(г) = -393,51;
∆Н°(Н2О(ж)) = -285,83) находим:
∆Н°(С2Н2) =
= 2(-393,51) + (-285,83) + 1299,65 = 226,8 кДж.
Ответ: ∆Н°(С2Н2) = 226,8 кДж.
1По табличным данным при 0 оС: ∆Н°(О3) = 144,457 кДж/моль. Можно отнести это на счет погрешностей при использовании данных для нормальных условий, т.е. при t = 20 - 25 oC.

