Строение атомов элементов подгруппы марганца и галогенов
Задача 1095.
Указать различия в строении атомов элементов подгруппы марганца и галогенов. В какой степени окисленности эти элементы проявляют наибольшее сходство в свойствах?
Решение:
Общая электронная формула валентных подуровней элементов VIIА-подгруппы ns2пр5. Общая электронная формула валентных подуровней элементов подгруппы марганца nd5пs2. Так как на внешнем уровне атомов элементов подгруппы галогенов имеется по семь электронов, а у подгруппы марганца - по два электрона. Первые - типичные неметаллы, а вторые - металлы. Но у элементов этих подгрупп есть и общие свойства: вступая в химические реакции, все они (за исключением фтора F)могут отдавать по 7 электронов на образование химических связей. При этом атомы подгруппы марганца отдают 2 электрона с внешнего и 5 электронов со следующего за ним уровня. Таким образом, у элементов побочных подгрупп валентными являются электроны не только внешних, но и предпоследних (вторых снаружи) уровней, в чем состоит основное различие в свойствах элементов главных и побочных подгрупп. Все галогены имеют структуру внешней электронной оболочки s2p5. Поэтому они легко принимают электрон, образуя устойчивую благородногазовую электронную оболочку (s2р6).
К подгруппе марганца принадлежат марганец, технеций и рений. В отличии от галогенов элементы подгруппы марганца имеют на внешнем электронном уровне всего два электрона и поэтому не проявляют способности присоединять электроны, образуя отрицательно заряженные ионы. Элементы главной и побочной подгрупп VII группы проявляют наибольшее сходство в свойствах, проявляя степени окисленности +7.
Окислительно-восстановительные свойства перманганата калия
Задача 1096.
Какая масса перманганата калия потребуется для окисления 7,60 г FeSO4 в нейтральном и в кислом растворах?
Решение:
M(FeSO4) = 152 г/моль;
M(KMnO4) = 158 г/моль.
а) В окислительно-восстановительном процессе между FeSO4 и KMnO4 в нейтральной среде проходят следующие процессы:
MnO4– + 3 ⇒ MnO2;
⇒ MnO2;
Fe2+ - 1 ⇒ Fe3+
⇒ Fe3+
Таким образом, марганец присоединяет 3 электрона, значит его эквивалентная масса KMnO4 равна М(KMnO4)/3. Так как железо отдает 1 электрон, то эквивалентная масса M(FeSO4)/1. По закону эквивалентов рассчитаем массу перманганата калия, которая потребуется для окисления 7,60 г FeSO4 в нейтральном растворе, получим:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
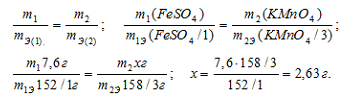
б) В окислительно-восстановительном процессе между FeSO4 и KMnO4 в кислой среде проходят следующие процессы:
MnO4– + 5 ⇒ Mn2+
⇒ Mn2+
Fe2+ - 1 ⇒ Fe3+
⇒ Fe3+
Таким образом, марганец присоединяет 5 электронов, значит его эквивалентная масса KMnO4 равна М(KMnO4)/5. Так как железо отдает 1 электрон, то эквивалентная масса M(FeSO4)/1. По закону эквивалентов рассчитаем массу перманганата калия, которая потребуется для окисления 7,60 г FeSO4 в нейтральном растворе, получим:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
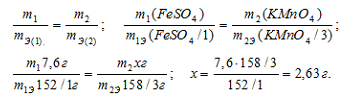
Ответ: 2,36г, 1,58г.

