Количественное осаждение хлорида калия нитратом серебра
Задача 137.
Написать уравнения реакции осаждения, рассчитать объём осадителя, необходимый для проведения количественного осаждения, и описать условия осаждения. Исследуемое вещество KCl, навеска массой 1,50 г; осадитель AgNO3, концентрация 10%.
Решение:
Схема реакции осаждения:
KCl + AgNO3 = AgCl↓ + KNO3
Так как вещества реагируют в химических реакциях равным числом грамм-эквивалентов, то
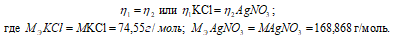
Согласно закону равенства эквивалентов:
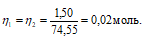
Рассчитаем массу AgNO3:
m(AgNO3) = MЭ(AgNO3) . n(AgNO3) =
= (74,55 . 0,02) = 1,5 г.
Теперь рассчитаем объём раствора AgNO3, теоретически необходимый для осаждения 1,50 г KCl из пропорции:
100 : 10 = х : 1,5;
х = (1,5 . 100)/10 = 15 см3.
Для полного осаждения необходимо брать полуторный избыток раствора осадителя от теоретически расчётного, т.е. объём (BaCl2 . 2H2O, необходимый для осаждения:
V(BaCl2 . 2H2O) = (1,5 . 15) = 22,5 см3.
Условия осаждения:
Определение осложняется тем, что AgCl склонен к образованию очень мелких кристаллов, проходящих через поры фильтра, что затрудняет фильтрование и приводит к потерям. Поэтому в начале осаждения создают условия, обеспечивающие получение крупных кристаллов:
- медленно прибавляют осадитель, что необходимо также и для получения более чистого осадка;
- повышают температуру раствора, что, в свою очередь, также повышает растворимость осадка.
Для обеспечения полноты осаждения в конце процесса добавляют избыток осадителя, фильтрование осадка проводят после охлаждения раствора.
Ответ: V(AgNO3) = 22,5 см3.
Задача 138.
Написать уравнения реакции осаждения, рассчитать объём осадителя, необходимый для проведения количественного осаждения, и описать условия осаждения. Исследуемое вещество KCl, навеска массой 0,90 г; осадитель AgNO3, концентрация 0,2 N.
Решение:
Схема реакции осаждения:
KCl + AgNO3 = AgCl↓ + KNO3
Так как вещества реагируют в химических реакциях равным числом грамм-эквивалентов, то
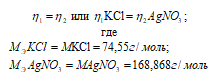
Согласно закону равенства эквивалентов:
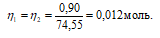
Теперь рассчитаем объём раствора AgNO3, теоретически необходимый для осаждения 0,90г KCl из пропорции:
1000 : 0,2 = х : 0,012;
х = (0,012 . 1000)/0,2 = 60 см3.
Для полного осаждения необходимо брать полуторный избыток раствора осадителя от теоретически расчётного, т.е. объём (BaCl2 . 2H2O, необходимый для осаждения:
V(BaCl2 . 2H2O) = (1,5 . 60) = 90 см3.
Условия осаждения:
Определение осложняется тем, что AgCl склонен к образованию очень мелких кристаллов, проходящих через поры фильтра, что затрудняет фильтрование и приводит к потерям. Поэтому в начале осаждения создают условия, обеспечивающие получение крупных кристаллов:
- медленно прибавляют осадитель, что необходимо также и для получения более чистого осадка;
- повышают температуру раствора, что, в свою очередь, также повышает растворимость осадка.
Для обеспечения полноты осаждения в конце процесса добавляют избыток осадителя, фильтрование осадка проводят после охлаждения раствора.
Ответ: V(AgNO3) = 90 см3.

