Определение типа гибридизации АО центрального атома комплексных иона
Задача 745.
Почему бесцветны ионы Аg+ и Zn2+?
Решение:
Ион серебра Ag+ имеет электронную конфигурацию (… 4d10). Все 4d – орбитали заполнены, и переход электронов с 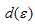 на
на 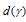 на
на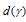 подуровень невозможен. Ион цинка Zn2+ имеет электронную конфигурацию (… 3d10). Все 3d-орбитали заполнены, и переход электронов с
подуровень невозможен. Ион цинка Zn2+ имеет электронную конфигурацию (… 3d10). Все 3d-орбитали заполнены, и переход электронов с 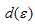 на
на 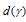 подуровень тоже невозможен, что можно представить в виде схемы:
подуровень тоже невозможен, что можно представить в виде схемы:
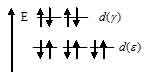
Поэтому ионы серебра и цинка не имеют окраски в водных растворах.
Задача 746.
Какой тип гибридизации АО центрального атома реализуется в ионе [Fe(F)6]4-, если значение магнитного момента этого иона свидетельствует о наличии в нем четырех неспаренных электронов?
Решение:
Электронная конфигурация иона Fe2+ (...3s23p63d6). Графическая схема заполнения электронами валентных орбиталей, в соответствии с правилом Хунда, будет иметь вид:
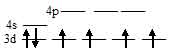
Ион [Fe(F)6]4- парамагнитен так как на 3d – орбиталях содержатся неспаренные электроны, а акцепторные орбитали (эти орбитали обозначены крестиком) служат одна 4s- и три 4р – орбитали иона Fe2+:
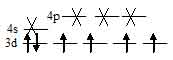
Таким образом, образование иона [Fe(F)6]4- сопровождается sp3 – гибридизацией АО железа. Пространственная структура этого иона – тетраэдр.
Задача 747.
Ион [Ni(NH3)6]2+ парамагнитен. Определить тип гибридизации АО иона Ni2+.
Решение:
Электронная конфигурация иона Ni2+ (...3s23p63d8). Графическая схема заполнения электронами валентных орбиталей, в соответствии с правилом Хунда, будет иметь вид:
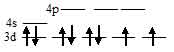
Ион [Ni(NH3)6]2+ парамагнитен так как на 3d – орбиталях содержатся неспаренные электроны, а акцепторные орбитали (эти орбитали обозначены крестиком) служат одна 4s- и три 4р – орбитали иона Fe2+:
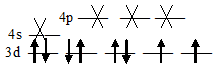
Таким образом, образование иона [Ni(NH3)6]2+ сопровождается sp3 – гибридизацией АО железа. Пространственная структура этого иона – тетраэдр.
Задача 748.
Ион [Fe(CN)6]4- диамагнитен. Доказать тип гибридизации АО иона Fe2+.
Решение:
На 3d – подуровне иона Fe2+ находятся шесть электронов, из них четыре неспаренных:
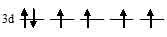
Лиганд сильного поля (СN) при образовании иона [Fe(CN)6]4- вызывает значительное расщепление d – подуровня и энергия расщепления столь значительна, что превысит энергию межэлектронного отталкивания спаренных электронов. В этом случае энергетически наиболее выгодно размещение всех шести электронов d – орбитали на 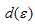 - подуровне в соответствии со схемой:
- подуровне в соответствии со схемой:
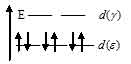
В результате в ионе [Fe(CN)6]4- все электроны оказываются спаренными, сам ион - диамагнитен. Электронная конфигурация иона Fe2+ (...3s23p63d6). Графическая схема заполнения электронами валентных орбиталей, в соответствии с правилом Хунда, будет иметь вид:
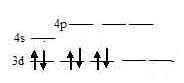
Ион [Fe(CN)6]4- диамагнитен так как на трёх 3d – орбиталях происходит спаривание шести электронов и освобождение двух d- орбиталей. Акцепторные орбитали (эти орбитали обозначены крестиком) служат одна 4s- и три 4р – орбитали и две 3d - орбитали иона Fe2+:
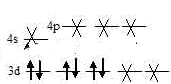
Таким образом, образование иона [Fe(CN)6]4- сопровождается d2sp3 – гибридизацией АО железа. Пространственная структура этого иона – октаэдр.
Задача 749.
Какова пространственная структура иона [Cu(NH3)4]2+ Каковы магнитные свойства этого иона?
Решение:
На 3d – подуровне иона Cu2+ находятся девять электронов, из них один неспаренный:
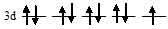
Лиганд сильного поля (NH3) при образовании иона [Cu(NH3)4]2+ вызывает значительное расщепление d – подуровня и энергия расщепления столь значительна, что превысит энергию межэлектронного отталкивания спаренных электронов. В этом случае энергетически наиболее выгодно размещение шести электронов d – орбитали на 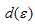 - подуровне и трёх электронов на
- подуровне и трёх электронов на 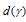 в соответствии со схемой:
в соответствии со схемой:
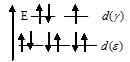
В результате в ионе [Cu(NH3)4]2+ содержится восемь спаренных электронов и один неспаренный, который и сообщает парамагнитные свойства. Электронная конфигурация иона Cu2+ (...3s23p63d9). Графическая схема заполнения электронами валентных орбиталей, в соответствии с правилом Хунда, будет иметь вид:
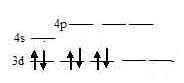
Ион [Cu(NH3)4]2+ парамагнитен, следовательно, в нём сохраняется один неспаренный электрон на d – подуровне, а акцепторные орбитали (эти орбитали обозначены крестиком) служат одна 4s- и три 4р – орбитали иона Cu2+:
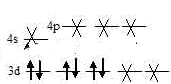
Таким образом, образование иона [Cu(NH3)4]2+ сопровождается sp3 – гибридизацией АО меди. Пространственная структура этого иона – тетраэдр.
Ответ: Тетраэдр, парамагнитен.

