Расчет концентрации ионов водорода в растворе кислоты
Задача 511.
Вычислить концентрацию ионов [H+] в 0,02 М растворе сернистой кислоты. Диссоциацией кислоты во второй ступени пренебречь.
Решение:
K1(H2SO3) = 1,6 . 10-2.
Рассчитаем степень диссоциации кислоты по уравнению: KD = CM .  2, где
2, где
KD – константа диссоциации кислоты, СМ – молярная концентрация кислоты,  - степень диссоциации кислоты, получим:
- степень диссоциации кислоты, получим:
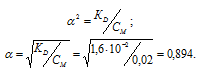
Концентрация иона водорода будет равна произведению степени диссоциации на концентрацию кислоты:
[H+] = . CM = 0,894 . 0,02 =
. CM = 0,894 . 0,02 =
= 0,018 моль/л.
Ответ: 0,018 моль/л.
Задача 512.
Вычислить концентрацию ионов [H+], [HSe-] и [Se2-] в 0,05 М растворе H2Se.
Решение:
Уравнение диссоциации H2Se имеет вид:
H2Se ⇔ [H+] + [HSe-]
Константа диссоциации H2Se равна 1,7 . 104. Рассчитаем степень диссоциации кислоты по уравнению: KD = CM .  2, где
2, где
KD – константа диссоциации кислоты, СМ – молярная концентрация кислоты,  - степень диссоциации кислоты, получим:
- степень диссоциации кислоты, получим:
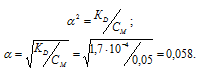
Концентрация иона водорода будет равна произведению степени диссоциации на концентрацию кислоты:
[H+] = [HSe-] =  . CM = 0,058 . 0,05 =
. CM = 0,058 . 0,05 =
= 0,0029 = 2,9 . 10-3.
Уравнение диссоциации H2Se по второй ступени имеет вид:
HSe- ⇔ H+ + Se2-.
Тогда выражение константы диссоциации иона HSe- будет иметь вид:
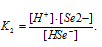
Отсюда
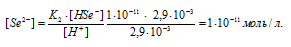
Ответ: [H+] = [HSe-] = 2,9 . 10-3; [Se2-] = 1 . 10-11.
Задача 513.
Во сколько раз уменьшится концентрация ионов водорода, если к 1 л 0,005 М раствора уксусной кислоты добавить 0,05 моля ацетата натрия?
Решение:
Исходную концентрацию ионов H+ в растворе (до добавления ацетата натрия( рассчитаем по уравнению:
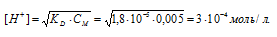
Концентрацию ионов водорода в растворе после добавления соли обозначим через x. Тогда, концентрация недиссоциированных молекул кислоты будет равна (0,005 –x). Концентрация ацетат-ионов будет слагаться из двух величин: из концентрации, создаваемой диссоциацией молекул кислоты (CH3COOH ⇔ CH3COO- + H+), и концентрации, обусловленной диссоциацией в растворе соли (CH3COONa ⇔ CH3COO- + Na+ ). Первая из этих величин равна x, а вторая – 0,005 моль/л; общая концентрация ионов CH3COO- равна, следовательно, (0,005 + x) моль/л. Подставив значения концентраций в выражение для константы диссоциации уксусной кислоты, получим:
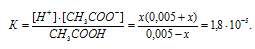
Так как в присутствии одноимённых ионов CH3COO- диссоциация уксусной кислоты подавляется, то степень её диссоциации мала и значением x можно пренебречь. Тогда последнее выражение упростится, получим:
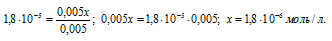
При сравнении исходной концентрации ионов водорода с рассчитанной, находим, что прибавление к раствору кислоты соли вызвало уменьшение концентрации ионов водорода в 167 раз:
(3 . 10-4)/(1,8 . 10-6) = 167
Ответ: в 167 раз.

