Вычисление значений рН для буферных растворов
Задача 80.
Рассчитать рН и степень диссоциации СН3СООН в 0,2 М растворе.
Решение:
KD(CH3COOH) = 1,78 · 10–5;
СМ(CH3COOH) = 0,2 М;
рН = ?
α = ?
1. Расчет рН и степени диссоциации СН3СООН в 0,2 М растворе до смешения с СН3СООNа
CH3COOH – слабая кислота. Для слабых кислот [H+] вычисляется по формуле:
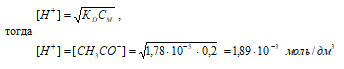
рН = –lg[H+] = –lg1,89 · 10–3 = 3 – lg1,89 = 2,72.
2. Расчет степени диссоциации кислоты
Для расчета расчета степени диссоциации кислоты будем использовать формулу: [H+] = СМ · α
Тогда
α = [H+]/CM(CH3COOH) = (1,89 · 10–3)/0,2 =
= 0,00945 или 0,945%.
Ответ: рН = 2,72 и α = 0,945%.
Задача 81.
Рассчитайте рН раствора, если к 100 см3 0,0375 М раствора СН3СООН прибавили СН3СООNа массой 0,1020 г.
Решение:
V(p-pa) = 100 см3;
KD(СН3СООН) = 1,78 · 10–5;
CM(СН3СООН) = 0,0375 М;
m(СН3СООNa) = 0,1020 г;
М(СН3СООNa) = 82,03 г/моль.
pH = ?
1. Рассчитаем молярность СН3СООNа
СМ(СН3СООNa) = [m(СН3СООNa) · 1000/100]/М(СН3СООNa) =
= 1,020/82,03 = 0,0124 M.
2. Рассчитаем концентрацию ионов водорода в растворе
Для буферных растворов, образованных слабой кислотой и солью этой кислоты, [Н+] находят по формуле:
[H+] = Кк · (Ск/Cс);
Тогда
[H+] = KD(СН3СООН) ·[СM(СН3СООН)/СM(СН3СООNa)] =
= 1,78 · 10–5 · (0,0375/0,0124) = 5,38 · 10–5 моль/дм3.
3. рассчитаем рН буферного раствора
рН = –lg[H+]; pH = –lg5,38 · 10–5 = 5 – lg5,38 = 4,27.
Ответ: 4,27.
Задача 82.
Вычислите концентрацию ионов Н+, ОН– и рН раствора, полученного смешением 25 см3 0,2 М раствора СН3СООН и 15 см3 0,1 М раствора СН3СООNа.
Решение:
KD(СН3СООН) = 1,78 · 10–5;
СМ(СН3СООН) = 0,2 М;
V(СН3СООН) = 25 см3;
СМ(СН3СООNа) = 0,1 М;
V(СН3СООNа) = 15 см3;
pH = ?
[H+] = ?
[OH–] = ?
Объём раствора, полученного после сливания исходных растворов, равен 40 cм3 [V(p-pa) = 25 + 15 = 40 см3].
Рассчитаем молярность веществ в полученном растворе смеси, получим:
СM(СН3СООН) = [СM(СН3СООН) · V(СН3СООН)]/V(p-pa) =
= (0,2 · 25)/40 = 0,125 моль/дм3;
СM(СН3СООNa) = [СM(СН3СООNa) · V(СН3СООNa)]/V(p-pa) =
= (0,1 · 15)/40 = 0,0375 моль/дм3.
Для буферных растворов, образованных слабой кислотой и солью этой кислоты, [Н+] находят по формуле:
[H+] = Кк · (Ск/Cс);
Тогда
[H+] = KD(СН3СООН) ·[СM(СН3СООН)/СM(СН3СООNa)] =
= 1,78 · 10–5 . (0,125/0,0375) = 5,93 · 10–5 моль/дм3
рН = –lg[H+]; pH = –lg5,93 · 10–5 = 5 – lg5,93 = 4,23.
Тогда
рН + рОН = 14;
рОН = 14 - рН = 14 - 4,23 = 9,77.
Отсюда
рОН = -lg[OH–];
[OH–] = 10-9,77 = 1,69 · 10–10 моль/дм3.
Ответ: [Н+] = 5,93 · 10–5 моль/дм3; [ОН–] = 1,69 · 10–10 моль/дм3; рН = 4,23.

