"Химия. 9 класс". О.С. Габриелян
Общая характеристика химических элементов. Амфотерность
Вопрос 1.
Амфотерными гидроксидам присуще свойство реагировать с кислотами как основание и со щелочами как кислота. Поэтому, когда мы к раствору щелочи приливаем по каплям раствор соли, у нас получается амфотерный гидроксид, который сразу же реагирует с щелочью, образуя растворимую соль, и мы не наблюдаем выпадение в осадок амфотерного гидроксида.
Вопрос 2.
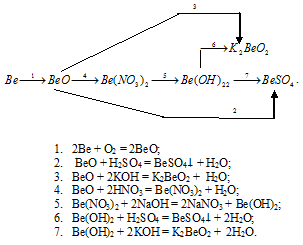
Вопрос 3.
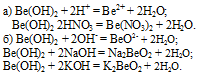
Вопрос 4.
Амфотерностью называется способность вещества проявлять как кислотные, так и основные свойства. Кислотные свойства, как правило, проявляют соединения неметаллов.
Например, HNO3, HCl, CO2, SO3,P2O5.
Но также существуют и кислоты, образованные металлами:
HMnO4 – марганцовая кислота, её соль – KMnO4 – перманганат калия; H2Cr2O7 – двухромовая кислота и её соль K2Cr2O7 – бихромат калия;
H3VO4 – ванадиевая кислота и её соль Na3VO4 – ванадат натрия;
K[AlOH)4] – тетрагидроксоалюминат калия, соль – соль алюминиевой кислоты. То есть металлы могут также проявлять кислотные свойства. Основные свойства характерны практически только для металлов. Например, KOH, NaOH, Ca(OH)2, Ba(OH)2, CaO, Li2O, KNO3.

