Вычисление длины диполя и дипольного момента молекулы
Задача 254.
Дипольный момент молекулы HCN равен 2,9 D. Вычислить длину диполя.
Решение:
Дипольный момент молекулы равен произведению абсолютного значения заряда электрона g (1,60 . 10-19 Кл) на расстояние l между центрами положительного и отрицательного зарядов в диполе:
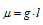
Отсюда
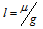
Учитывая, что 1 D = 3,33 . 10-30 Кл . м, находим длину диполя:
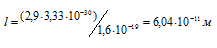
Ответ: 6,04 . 10-11 м.
Задача 255.
Длина диполя молекулы фтороводорода равна 4 . 10-11 м. Вычислить ее дипольный момент в дебаях и в кулон-метрах.
Решение:
Дипольный момент молекулы равен произведению абсолютного значения заряда электрона g (1,60 . 10-19 Кл) на расстояние l между центрами положительного и отрицательного зарядов в диполе:
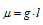
Дипольный момент измеряют в дебаях (D), 1D = 3,33 . 10-30 Кл . м).
Находим дипольный момент молекулы в кулон-метрах:
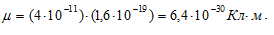
Вычисляем дипольный момент молекулы в дебаях:
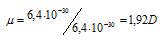
Ответ: 6,04 . 10-30 Кл . м = 1,92 D.
Задача 256.
Дипольные моменты молекул Н2О и Н2S равны соответственно 1,84 и 0,94 D. Вычислить длины диполей. В какой молекуле связь более полярна? Указать направления дипольных моментов связей в этих молекулах.
Решение:
Дипольный момент молекулы равен произведению абсолютного значения заряда электрона g (1,60 . 10-19 Кл) на расстояние l между центрами положительного и отрицательного зарядов в диполе:
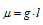
Дипольный момент измеряют в дебаях (D), 1D = 3,33 . 10-30 Кл . м).
Вычислим длину связи молекулы Н2О:
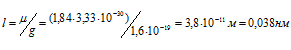
Вычислим длину связи молекулы H2S:
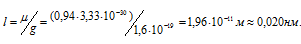
Так как дипольный момент молекулы Н2О больше, чем молекулы H2S, то в молекуле Н2О связь более полярна. Учитывая, что атомы кислорода и серы более электроотрицательнее атома водорода, то дипольные моменты связей будут направлены от атома водорода соответственно к атому кислорода и серы (Н→ О, H →S).
Ответ: 0,038 и 0,020 нм.
Задача 257.
Описать пространственное строение неполярной молекулы ВеСI2. Какие АО бериллия участвуют в образовании связей Ве—С1?
Решение:
В молекуле BeCl2 валентный электронный слой атома бериллия содержит две электронных пары:
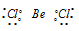
Поэтому электронные облака атома бериллия будут максимально удалены друг от друга при sp-гибридизации, когда их оси совпадают и направлены противоположно друг к другу, что приводит к нулевому значению дипольного момента, молекула приобретает линейное строение:
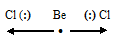
При образовании молекулы BeCl2 в образовании связей Be—Cl участвуют две sp-гибридные АО бериллия.
Задача 258.
Дипольный момент молекулы SO2 равен 1,бI D, молекулы СО2 - нулю. Одинаковы ли валентные углы ОSО и ОСО? Ответ мотивировать.
Решение:
Дипольный момент – величина векторная, направленная от положительного конца диполя к отрицательному. Поэтому дипольный момент многоатомной молекулы следует рассматривать как некоторую сумму дипольных моментов связей; она зависит не только от полярности каждой связи, но и от взаимного расположения этих связей.
В линейных молекулах типа АВ2, в нашем случае в молекуле СО2, дипольные моменты связей С=О направлены друг к другу и поэтому взаимно компенсируются, что и приводит к нулевому значению суммарного диполя молекулы. Поэтому углы ОСО равны 1800. Схема молекулы СО2 имеет вид:
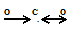
Так как дипольный момент молекулы SO2 имеет значение больше нуля, то дипольные моменты связей S—O направлены друг к другу под углом, молекула имеет угловую структуру:
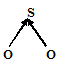
Взаимное расположение связей в молекуле SO2 угловое, т.е. молекула построена в форме треугольника. Поэтому валентные углы ОSО и ОСО не одинаковы.
Задача 259.
Дипольный момент молекулы СS2 равен нулю. Каким типом гибридизации АО углерода описывается образование этой молекулы?
Решение:
Электронная конфигурация атома углерода 1s22s22р2. Электронное строение его валентных орбиталей в стационарном состоянии может быть представлено следующей схемой:
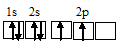
Электронное строение валентных орбиталей атома углерода в возбужденном состоянии представлено следующей схемой:
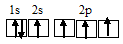
Четыре неспаренных электрона возбуждённого атома углерода могут участвовать в образовании четырёх ковалентных связей по обычному механизму с другими атомами химических элементов. Так как дипольный момент молекулы CS2 равен нулю, то молекула имеет линейное строение. В CS2 валентный электронный слой содержит четыре пары электронов, по две пары с двух сторон атома углерода:
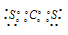
Поэтому в молекуле CS2 углерод находится в состоянии sp-гибридизации. Образовавшиеся равноценные sp-гибридные орбитали образуют одинарные  - связи C—S, а два неспаренных р-облака, перекрываясь образуют
- связи C—S, а два неспаренных р-облака, перекрываясь образуют  - связь с атомами серы. Поэтому в молекуле CS2 sp-гибридные облака ориентируются в противоположных направлениях, молекула имеет линейное строение. В линейных молекулах типа АВ2, в нашем случае в молекуле CS2, дипольные моменты связей С=S направлены друг к другу и поэтому взаимно компенсируются, что и приводит к нулевому значению суммарного диполя молекулы. Поэтому углы SСS равны 1800. Схема молекулы СS2 имеет вид:
- связь с атомами серы. Поэтому в молекуле CS2 sp-гибридные облака ориентируются в противоположных направлениях, молекула имеет линейное строение. В линейных молекулах типа АВ2, в нашем случае в молекуле CS2, дипольные моменты связей С=S направлены друг к другу и поэтому взаимно компенсируются, что и приводит к нулевому значению суммарного диполя молекулы. Поэтому углы SСS равны 1800. Схема молекулы СS2 имеет вид:
S → C ← S
Задача 260.
Дипольные моменты молекул ВF3 и NF3 равны соответственно О и 0,2 D. Какими типами гибридизации AO бора и азота описывается образование этих молекул?
Решение:
а) В молекуле BF3 валентный электронный слой атома бора содержит три пары электронов:
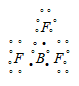
Электронные облака атома бора будут максимально удалены друг от друга при sp2-гибридизации, когда оси связей
B—F направлены друг к другу под углом 1200 (т.е. в направлениях к вершинам правильного треугольника), молекула будет иметь форму:
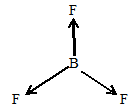
Такое расположение связей взаимно компенсирует их дипольные моменты, так что суммарное значение дипольного момента молекулы трифторида бора равно нулю.
б) В молекуле NF3 валентный электронный слой атома азота содержит четыре пары электронов:
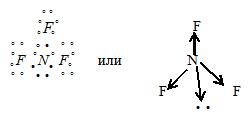
Поэтому электронные облака атома азота будут максимально удалены друг от друга при sp3-гибридизации, когда оси связей N—F будут направлены к вершинам тетраэдра (углы между этими направлениями составляют 109028’). При образовании молекулы NF3 атом азота расположен в центре тетраэдра, а атомы фтора расположены в трёх вершинах тетраэдра, к четвёртой вершине направлено электронное облако неподелённой пары электронов атома азота. Образовавшаяся фигура – тригональная пирамида. Дипольный момент такой молекулы будет иметь значение больше нуля.

