Решение задачи на определение формулы алкена
Задача 1.39.
Относительная плотность паров некоторого алкена по водороду 21. Определите его молекулярную формулу.
Дано:
относительная плотность паров алкена по водороду: D(H2) =21.
Найти: молекулярную формулу углеводорода.
Решение:
Шаг 1. В состав углеводорода входит только углерод и водород. Для гомологического ряда алкенов известна общая формула, в которой индексы у углерода и водорода связаны между собой: СkН2k. Неизвестной является только одна переменная k.
Шаг 2. В условии нет указаний на химическую реакцию.
Шаг 3. Мы также пропускаем, так как соотношение атомов углерода и водорода уже известно из общей формулы алкена.
Шаг 4. Простейшая формула легко определяется по общей формуле путем подстановки вместо «k» значения «1»: С1Н2.
Шаг 5. Выявление истинной формулы.
Вещества с формулой СН2 не существует. В истинной формуле индексы будут в некоторое число раз больше, чем в простейшей. Для определения, во сколько раз необходимо увеличить индексы в простейшей формуле, необходимо определить значение истинной молярной массы искомого вещества. Для этого по данным об относительной плотности паров искомого вещества по водороду определяем истинную молярную массу.
Воспользуемся соотношением:
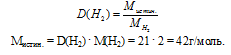
Определим значение молярной массы для простейшей формулы:
Мпрост. = 1 . 12 + 2 . 1 = 14 г/моль.
Истинная молярная масса больше молярной массы простейшей формулы, следовательно, индексы в простейшей формуле необходимо увеличивать.
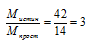
Умножаем индексы в простейшей формуле на «3» и получаем истинную формулу: С3Н6 . М(С3Н6) = 42 г/моль.
Ответ: С3Н6 (пропен).

