Определение формулы оксида с использованием последовательно-разветвленного, так и встречного алгоритмов
Задача 158.
Массовая доля кислорода в оксиде некоторого элемента составляет 56,34% . Определите формулу этого оксида.
Дано: массовая доля кислорода: (О)(в оксиде) = 56,34% .
Найти: формулу оксида.
Решение:
В данной задаче также возможен как последовательно-разветвленный, так и встречный алгоритм. Рассмотрим оба способа решения.
I способ (последовательно-разветвленный алгоритм).
В аналогичном примере решения такой задачи (№ 1.115) мы применили следующий алгоритм:
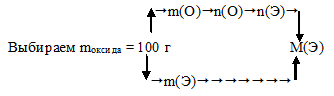
Для определения количества вещества искомого элемента по количеству вещества кислорода (переход n(О) → n(Э)) мы пользовались индексами в общей формуле искомого вещества. В данном случае в условии нет данных, позволяющих определить эти индексы. Следовательно, решение данной задачи возможно только путем подбора индексов в формуле. Для этого необходимо перебрать все возможные степени окисления (с.о.) неизвестного элемента и по ним составить общую формулу. По определению класса оксидов искомый элемент может проявлять степени окисления, выражающиеся положительными целыми числами. Максимальная степень окисления определяется химическими свойствами и ограничивается значением (+8). Наш алгоритм на этом этапе (n(О) ⇔ n(Э)) будет иметь альтернативный характер:
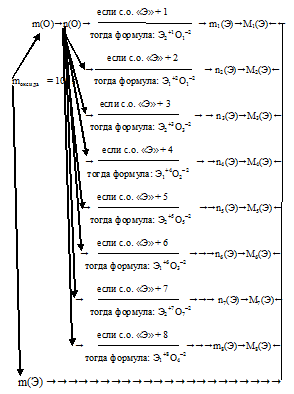
При каждом значении степени окисления (с.о.) мы определяем молярную массу искомого элемента и сопоставляем ее с массовыми числами в Периодической системе. Решением будет являться тот вариант, при котором вычисленное значение молярной массы совпадет со значением молярной массы какого-либо элемента. Причем найденный элемент должен реально проявлять использованную при его расчете степень окисления.
Выбираем образец массой 100 г. В нем содержится 56,34 г кислорода (по значению массовой доли кислорода).
Определяем массу искомого элемента в выбранном образце:
m(Э) = 100 – m(О) = 100 – 56,34 = 43,66 г.
Находим количество вещества атомарного кислорода:
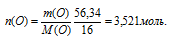
Приступим к перебору степеней окисления:
а) Пусть степень окисления искомого элемента (+1), тогда формула оксида будет иметь вид Э2О.
n(Э+1) > п(О–2) в 2 раза (по индексам в предполагаемой формуле)
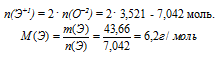
По Периодической системе находим элемент с молярной массой атомов 6,2 г/моль. Наиболее близка молярная масса лития: М(Li) = 6,9 г/моль. Он проявляет степень окисления (+1) при образовании оксида Li2О, но согласование между расчетной молярной массой и табличной не очень удовлетворительно. Поэтому в данном случае разумно продолжить перебор. Переходим к следующему значению степени окисления.
б) Пусть степень окисления искомого элемента (+2), тогда формула оксида будет иметь вид ЭО.
n(Э+2) = п(О–2) (по индексам в предполагаемой формуле)
n(Э+2) = 3,521 моль.
<
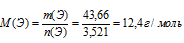
По Периодической системе находим элемент с молярной массой атомов 12,4 г/моль. Наиболее близка молярная масса атомов углерода: М(С) — 12 г/моль. Он проявляет степень окисления (+2) при образовании оксида СО. В данном случае согласование между расчетной молярной массой и табличной лучше, чем для лития, но не идеально. Поэтому разумно продолжить перебор. Переходим к следующему значению степени окисления.
в) Пусть степень окисления искомого элемента (+3), тогда формула оксида будет иметь вид Э2О3.
на 2 моль Э+3 приходится 3 моль (О2–) по записи формулы)
на х моль Э+3 приходится 3,521 моль (О2–) (по условию)</p>
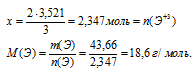
По Периодической системе находим элемент с молярной массой атомов 18,6 г/моль. Наиболее близка молярная масса атомов фтора: М(F) = 19 г/моль.
Но фтор с кислородом образует не оксид, а фторид кислорода (ОГ2 ) и проявляет в нем степень окисления (–1), следовательно, этот вариант не подходит вовсе. Переходим к следующему значению степени окисления.
г) Пусть степень окисления искомого элемента (+4), тогда формула оксида будет иметь вид ЭО2.
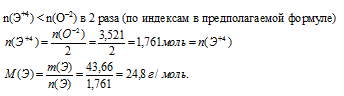
По Периодической системе находим элемент с молярной массой атомов 24,8 г/моль. Наиболее близка молярная масса атомов магния: M(Мg) = 24,3 г/моль. Но магний не проявляет степень окисления (+4), следовательно, этот вариант не подходит. Переходим к следующему значению степени окисления.
д) Пусть степень окисления искомого элемента (+5), тогда формула оксида будет иметь вид Э2О5.
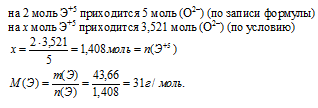
По Периодической системе находим элемент с молярной массой атомов 31 г/моль. Идеально подходит молярная масса атомов фосфора: М(P) = 31 г/моль. Он проявляет степень окисления (+5) при образовании оксида Р2O5. В данном случае согласование между расчетной молярной массой и табличной идеальное, что позволяет однозначно определить правильный ответ: Р2О5.
Подобные задачи могут иметь несколько удовлетворяющих условию ответов. Поэтому в данном случае разумно перебрать все остальные значения степеней окисления до (+8).
е) Пусть степень окисления искомого элемента (+6), тогда формула оксида будет иметь вид ЭО3.
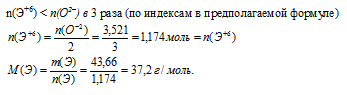
По Периодической системе находим элемент с молярной массой атомов 37,2 г/моль. Ни одно из значений массовых чисел не согласуется с рассчитанной молярной массой. Следует отметить, что один из распространенных природных изотопов хлора имеет молярную массу 37 г/моль. Но хлор не удовлетворяет условию согласования степени окисления. Он проявляет нечетные степени окисления, следовательно, этот вариант не подходит.
Переходим к следующему значению степени окисления.
ж) Пусть степень окисления искомого элемента (+7), тогда формула оксида будет иметь вид Э2О7.
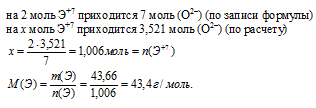
По Периодической системе находим элемент с молярной массой атомов 43,4 г/моль. Ни одно из значений массовых чисел не согласуется с рассчитанной молярной массой, следовательно, этот вариант не подходит. Переходим к следующему значению степени окисления.
з) Пусть степень окисления искомого элемента (+8), тогда формула оксида будет иметь вид ЭО4.
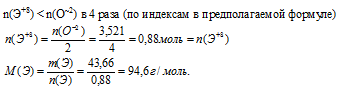
По Периодической системе находим элемент с молярной массой атомов 49,6 г/моль. Ни одно из значений массовых чисел не согласуется с рассчитанной молярной массой, следовательно, этот вариант не подходит.
Ответ: идеально согласуется с условием задачи Р2О5.
II способ (встречный алгоритм).
Встречный алгоритм решения выглядит следующим образом:
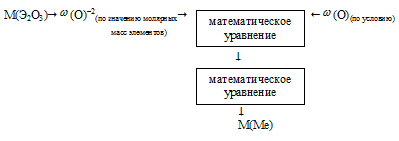
Этот алгоритм можно использовать без изменения и для решения данной задачи, но для его применения необходимо составить общую формулу искомого оксида. Обозначим неизвестную степень окисления искомого элемента буквенной переменной «k». В этом случае формула оксида будет иметь вид: Э2+kОk–2. Применим предложенный алгоритм.
Запишем выражение для молярной массы Э2+kОk–2:
М(Э2+kОk–2) = 2 . М(Э) + k . М(О) =
= (2 . М(Э) + k . 16) г/моль.
Масса 1 моль Э2+kОk–2составляет (2 . М(Э) + k . 16) г. Масса кислорода в ней (k . 16) г.
Составим выражение для массовой доли кислорода, используя данные, полученные по молярной массе.
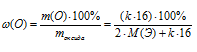
Приравниваем полученное выражение к значению массовой доли кислорода из условия
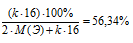
Получили одно уравнение с двумя неизвестными: М(Э) и «kс». Оно имеет множество решений, но нам необходимо выбрать лишь то, которое удовлетворяет физическому смыслу. Переменная «k» обозначает степень окисления неизвестного элемента и индекс в формуле, поэтому физическому смыслу могут удовлетворять значения целых положительных чисел от 1 до 8. Для нахождения верного ответа будем последовательно подставлять в полученное уравнение значения «k» и вычислять значения молярной массы искомого элемента М(Э). Далее будем сопоставлять ее с массовыми числами в Периодической системе. Решением будет являться тот вариант, при котором вычисленное значение молярной массы совпадет со значением молярной массы какого-либо элемента. Причем найденный элемент должен реально проявлять использованную при его расчете степень окисления.
Значения М(Э), полученные при решении уравнения отразим в таблице:
|
Степень |
M(Э), г/моль |
Согласование значений М(Э) и «k» с физическим смыслом |
| +1 | 6,,2 | Наиболее близка молярная масса атомов лития: М(Li) = 6,9 г/моль. Он проявляет степень окисления «+1» при образовании оксида Li2O, но согласование между расчетной молярной массой и табличной не очень удовлетворительно. |
| +2 | 12,4 | Наиболее близка молярная масса атомов углерода: М(С) = 12 г/моль. Он проявляет степень окисления «+2» при образовании оксида СО. В данном случае согласование между расчетной молярной массой и табличной лучше, чем для лития, но не идеально. |
| +3 | 18,6 | Наиболее близка молярная масса атомов фтора: М(F) = 19 г/моль. Но фтор с кислородом образует не оксид, а фторид кислорода ( ОF2) и проявляет в нем степень окисления «-1», следовательно, этот вариант не подходит вовсе.. |
| +4 | 24,8 | Наиболее близка молярная масса атомов магния: М(Мg) = 24,3 г/моль. Но магний не проявляет степень окисления «+4», ) следовательно, этот-вариант не подходит |
| +5 | 31 | Идеально подходит молярная масса атомов фосфора: М(Р) = 31 г/моль. Он проявляет степень окисления «+5» при образовании оксида Р2О5. В данном случае согласование между расчетной молярноймассой и табличной идеальное, что позволяет од- молярной массой и табличной лучше, чем для лития, но не идеально. |
| +6 | 37,2 | Ни одно из значений массовых чисел не согласуется с рассчитанной молярной массой. Следует отметить, что один из распространенных природных изотопов хлора имеет молярную массу 37 г/моль. Но хлор не удовлетворяет условию согласования степени окисления. Он проявляет нечетные степени окисления, следовательно, этот вариант не подходит. |
| +7 | 43,4 | Ни одно из значений массовых чисел не согласуется с рассчитанной молярной массой, следовательно, этот вариант не подходит |
| +8 | 49,6 | По Периодической системе находим элемент с молярной массой атомов 49,6 г/моль. Ни одно из значений массовых чисел не согласуется с рассчитанной молярной массой, следовательно, этот вариант не подходит |
Ответ: идеально согласуется с условием задачи Р2О5. Решение данной задачи позволяет сделать следующий вывод.При согласовании расчетных значений молярной массы и степени окисления должны обязательно выполняться два условия:
1.Элемент, с полученной в результате расчета молярной массой атомов, должен существовать в Периодической системе Д.И. Менделеева.
2. Удовлетворяющий условию элемент в действительности должен быть способен проявлять степень окисления, использованную при его вычислении в этом шаге подбора.
И только при выполнении обоих условий можно использовать найденный элемент для формирования ответа задачи. Если хотя бы одно из условий не выполняется, следует продолжить перебор степеней окисления неизвестного элемента. Здесь следует заметить, что вариантов перебора для каждого элемента не очень много. Причиной этому служит ряд ограничений, накладываемых химией. 1. Числовое значение степени окисления, как правило, является целочисленным. 2. Знак степени окисления: (+) или (-), неизвестного элемента часто можно определить по другим, известным элементам. 3. Положительные степени окисления могут принимать значения целых чисел от «+1» до «+8 ». 4. Отрицательные степени окисления, в большинстве случаев, укладываются в интервал целых значений от (-1) до (-4).
Задачи на определение формулы вещества:
1. Определение формулы соли
2. Определение формулы эфира
3. Определение формулы углеводорода
Комментарии:
На самом деле существуют соединения, в которых у некоторых элементов степень окисления не целочисленная. Например, К+1О–1/3 — озонид калия (степень окисления кислорода в нем –1/3); Nа+1О2–1/2 — а супероксид натрия (степень окисления кислорода в нем –1/2). Такие значения степеней окисления не противоречат определению этого понятия: степень окисления — условный заряд атома, вычисленный в предположении полностью ионной связи.
Но такие соединения встречаются относительно редко, и подобные задачи с их использованием не составляются.

