Расчеты по химическим уравнениям с участием газовых смесей
Задача 8.
Определите объем воздуха (н.у.) необходимый для полного сгорания 60 л (н.у.) метана (СН4).
Дано:
объем (н.у.) сгоревшего метана: V(СН4) = 60 л.
Найти:
объем (н.у.) расходовавшегося воздуха: Vвозд. = ?
Решение:
Данных, представленных в условии, явно недостаточно для решения задачи. Нам необходимо дополнительно знать количественный состав воздуха1.
В данном случае в реакции горения метана принимает участие только кислород. Все остальные компоненты представляют собой неактивные примеси. Записываем уравнение реакции:
СН4 + 2О2 = СО2 + 2Н2О.
Алгоритм решения можно представить следующим образом:
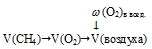
1. По уравнению горения определим объем кислорода, необходимого для сгорания 60 л метана.
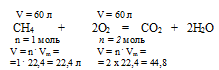
Составим пропорцию:
для сгорания 60 л (СН4) необходимо х л (О2) (по условию)
для сгорания 22,4 л (СН4) необходимо 44,8 л (О2) (по уравнению)
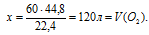
Можно было также найти объем кислорода по закону объемных отношений.
2. Используя дополнительную информацию о содержании кислорода в воздухе, определяем объем воздуха:
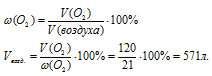
Ответ: 571 л воздуха (н.у.) потребуется для полного сгорания 60 л (н.у.) метана.
Задача 9.
Смесь азота и углекислого газа объемом 17,92 л (н.у.) пропустили через избыток раствора гидроксида калия. Определите массу образовавшейся соли, если относительная плотность исходной смеси газов по гелию была 9,5.
Дано:
объем газовой смеси: Vсмеси = 17,92 л;
относительная плотность смеси газов по гелию: D(Не) = 9,5.
Найти:
массу образовавшейся соли: mсоли = ?
Решение:
В данной смеси газов с гидроксидом калия взаимодействует только углекислый газ. Азот же является неактивной примесью. При избытке КОН в результате реакции получается средняя соль К2СО3:
CО2 + 2КОН = К2СО3 + Н2О.
Для определения массы образовавшейся соли нам необходимо по относительной плотности смеси газов найти количество СО2 в исходной смеси газов.
Алгоритм решения можно представить следующим образом:
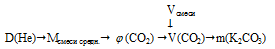
1. Определим среднюю молярную массу смеси газов.
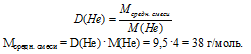
2. Определяем объемную долю СО2 в смеси.
Мсредн. смеси = М(СO2) . (СO2) + M(N2) . (N2)
(N2) = 1 – (СО2) (в долях от 1);
Мсредн. смеси = [М(СO2) . (СO2) + M(N2)] . [1 – (СО2)].
Подставляем все известные значения:
38 = 44 . [СO2+ 28(1 – (СO2)].
Решая это уравнение, получим (СO2) = 0,625.
3. Используя значение общего объема смеси газов, определяем объем (СО2).
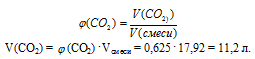
4. По уравнению реакции определяем массу полученной соли:
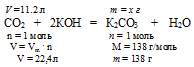
Составим пропорцию:
11,2л СО2 дают х г К2СO3 (по данным условия);
22,4 л СО2 дают 138 г К2СО3 (по уравнению).
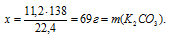
Ответ: = m(К2СО3) = 69 г.
Комментарии:
1 В условиях большинства задач с использованием воздуха его состав не указывается. Предполагается что решающий должен знать качественный и количественный состав воздуха либо хотя бы содержание в нем активного компонента, чаще всего кислорода.

