Определение формулы гидрофосфата аммония
Задача 1.3.
В некотором образце неорганического вещества содержится 36,061 г азота, 11,591 г водорода, 39,924 г фосфора и 82,424 г кислорода. Определите формулу этого соединения.
Дано:
масса азота: m(N) = 36,061 г;
масса водорода: m(Н) = 11,591 г;
масса фосфора: m(Р) = 39,924 г;
масса кислорода: m(О) = 82,424 г.
Найти: формулу вещества.
Решение:
Шаг 1. Из условия однозначно, следует, что вещество состоит из азота, водорода, фосфора и кислорода. Обозначим формулу как NxНyРzОk. Следовательно, требуется определить неизвестные индексы х, у, z, k.
Шаг 2. В условии нет указаний на химическую реакцию.
Шаг 3. Вычислим соотношение количеств веществ атомов (n) азота, водорода, фосфора и кислорода в данном образце. Используем соотношение: m = n . М.
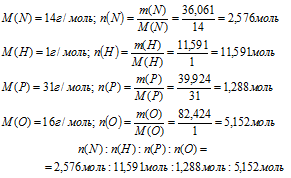
Шаг 4. Находим простейшую формулу.
Следуя выводу, сделанному при общем рассмотрении втоpого этапа (в начале 2 главы), можно записать:
N(N) : N(H) : N(Р) : N(О) =
= 2,576 : 11,591 : 1,288 : 5,152.
Выбираем наименьшее значение (в данном случае «1,288») и делим на него все четыре числа:
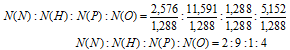
Получили набор наименьших целых чисел. Это дает возможность записать простейшую формулу: N2Н9Р1O4.
Шаг 5. Выявление истинной формулы.
Для придания формуле химического смысла воспользуемся информацией о классификации веществ. Соотношение фосфора и кислорода позволяет выделить кислотный остаток фосфорной кислоты (РО4)3–. Наличие азота, не входящего в состав кислотного остатка, позволяет предположить наличие аммониевых катионов (NН4)+. Два атома азота в полученной нами формуле указывает на то, что таких катионов тоже два. Но два аммонийных катиона содержат только 8 атомов водорода. Девятый атом водорода указывает на кислый характер соли (не все катионы водорода в фосфорной кислоте замещены на катионы аммония). Следовательно, химически осмысленная запись формулы искомого вещества будет выглядеть таким образом: (NН4)2НРО4.
Ответ: (NН4)2НРО4.
Задачи на определение формулы вещества:
1. Определение формулы углеводорода
2. Определение формулы алкена
3. Определение формулы алкана

