Вычисление процентного содержания сульфата железа и хлорида стронция в аналитическом образце вещества
Расчет процентного содержания сульфата железа в образце соли сульфата железа
Задача 177.
Вычислите процентное содержание определяемого вещества в аналитическом образце по следующим данным: исследуемое вещество сульфат железа, навеска массой 1,1200 г; определяемое вещество FeSO4; весовая форма Fe2O3, массой равной 0,7514 г.
Решение:
Расчёт процентного содержания определяемого вещества в пробе проводим по формуле:
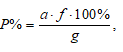
где
а - масса весовой формы определяемого вещества, г;
f - аналитический множитель (фактор пересчета);
g - масса навески, г;
Р - приблизительное процентное содержание вещества в образце.
Mr(Fe) = 55,845;
Mr(Fe2O3) = 159,69;
f = 2Mr(FeSO4)/Mr(Fe2O3) =
= (2 . 55,845)/159,69 = 0,6994.
Подставив все числовые значения в расчётную формулу, получим:
Р% = (0,7514 . 0,6994 . 100%)/1,1200 = 49,92%.
Ответ: Р% = 49,92%.
Вычисление процентного содержания хлорида стронция в образце соли хлорида стронция
Задача 178.
Вычислите процентное содержание определяемого вещества в аналитическом образце по следующим данным: исследуемое вещество стронция хлорид, навеска массой 0,7500 г; определяемое вещество SrCl2; весовая форма SrC2O4 . H2O, массой равной 0,3713 г.
Решение:
Расчёт процентного содержания определяемого вещества в пробе проводим по формуле:
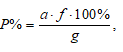
где
а - масса весовой формы определяемого вещества, г;
f - аналитический множитель (фактор пересчета);
g - масса навески, г;
Р - приблизительное процентное содержание вещества в образце.
Mr(SrCl2) = 158,526;
Mr(SrC2O4 . H2O) = 193,62;
f = Mr(SrCl2)/(SrC2O4 . H2O) =
= 158,526/193,62 = 0,8187.
Подставив все числовые значения в расчётную формулу, получим:
Р% = (0,3713 . 0,8187 . 100%)/0,7500 = 40,53%.
Ответ: Р% = 40,53%.
Задача 179.
Вычислите процентное содержание определяемого вещества в аналитическом образце по следующим данным: исследуемое вещество стронция хлорид, навеска массой 0,5712 г; определяемое вещество SrCl2; весовая форма SrC2O4 . H2O, массой равной 0,2712 г.
Решение:
Расчёт процентного содержания определяемого вещества в пробе проводим по формуле:
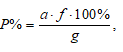
где
а - масса весовой формы определяемого вещества, г;
f - аналитический множитель (фактор пересчета);
g - масса навески, г;
Р - приблизительное процентное содержание вещества в образце.
Mr(SrCl2) = 158,526;
Mr(SrC2O4 . H2O) = 193,62;
f = Mr(SrCl2)/(SrC2O4 . H2O) =
= 158,526/193,62 = 0,8187.
Подставив все числовые значения в расчётную формулу, получим:
Р% = (0,2712 . 0,8187 . 100%)/0,5712 = 38,87%.
Ответ: Р% = 38,87%.

