Вычисление процентного содержания определяемого вещества в аналитическом образце
Задача 3.
Вычислите процентное содержание определяемого вещества в аналитическом образце по данным: анализируемый образец сталь, навеска массой 1,1213 г; определяемое вещество Fe; весовая форма Fe2O3, масса равна 0,2931 г.
Решение:
Расчёт процентного содержания определяемого вещества в пробе проводим по формуле:
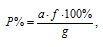
где
а - масса весовой формы определяемого вещества, г;
f - аналитический множитель (фактор пересчета);
a - масса навески, г;
Р - приблизительное процентное содержание вещества в образце.
ArFe = 55,84;
MrFe2O3 = 159,68;
f = 2 ArFe/ MrFe2O3 =
= (2 . 55,84)/159,68 = 0,6994.
Подставив все числовые значения в расчётную формулу, получим:
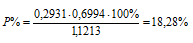
Ответ: Р% = 18,28%.
Задача 4
Вычислить потерю от растворимости осадка в граммах и процентах при промывании его указанным объёмом промывной жидкости. Осадок Ag2CO3, массой 0,30 г, ПрAg2CO3 =5,0 . 10-12; промывная жидкость Н2О, объёмом 50 см3.
Решение:
Вычислим растворимость в молях на 1 дм3 Ag2CO3, обозначив её через х, получим:
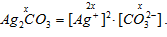
Произведение растворимости карбоната серебра - величина справочная ПрAg2CO3 =5,0 . 10-12, поскольку:
ПрAg2CO3 = [Ag+]2 . [CO32-] =
= x3 = 5,0 . 10-12
Откуда
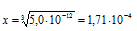
моль,
следовательно, в 250 см3 воды растворится следующее количество Ag2CO3: 1,71 . 10-4 0,25 = 4,275 . 10-5 моль Ag2CO3.
Найдём растворимость в 1 г/дм3, для этого необходимо молярную массу Ag2CO3 умножить на растворимость в моль/дм3, а поскольку МгAg2CO3 = 275,736, то потеря от растворимости при промывании равна:
4,275 . 10-5 . 275,736 =0,0118г.
Обычно потерю растворимости выражают в процентах, найдём её:
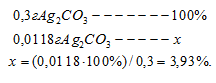
Таким образом, при промывании осадка Ag2CO3 250 см3 воды мы вносим очень большую погрешность (около 4%) в результате потерь от растворимости.
Задача 5
Вычислите аналитический множитель (фактор пересчета) для определения: определяемое вещество Na; весовая форма Na2SO4
Решение:
Аналитический множитель (фактор пересчета), является отношением молярных масс определяемого вещества и его весовой формы, взятых в соответствии с коэффициентами их образования, число атомов определяемого компонента в числителе и знаменателе дроби должно быть одинаковым. В рассматриваемом примере химическая эквивалентность соединений в числителе и знаменателе устанавливается простым уравниванием числа атомов определяемого элемента, общего для определяемого вещества (Na) и гравиметрической (весовой) формы (Na2SO4), то аналитический множитель будет иметь следующее значение:
f = 2ArNa/MrNa2SO4 =
=(2 . 23)/142 = 0,3239, где
ArNa = 23;
MrNa2SO4 = 142.
Ответ: f = 0,3239.

