Как очистить ртуть от примесей «неблагородных» металлов
Задача 1026.
Металлическая ртуть часто содержит примеси «неблагородных» металлов — цинка, олова, свинца. Для их удаления ртуть обрабатывают раствором Нg(NO3)2. На чем основан такой способ очистки ртути?
Решение:
Способ очистки ртути от «неблагородных» металлов основан на способности металлов, расположенных в ряду напряжений до ртути, вытеснять её из растворов её же солей. Например, если ртуть обработать раствором Нg(NO3)2, то, примеси, содержащие цинк, олово и свинец, будут вытеснять ртуть из её соли и переходить в раствор в виде нитратов. Таким образом при обработке ртути Нg(NO3)2, находящиеся в ртути в виде примесей цинк, олово и свинец перейдут в раствор, а металлическая ртуть останется без примесей «неблагородных» металлов. Рассмотрим химизм процесса очистки ртути на примере цинка, получим:
Zn + Hg(NO3)2 = Zn(NO3)2 + Hg.
Уравнения электронного баланса:
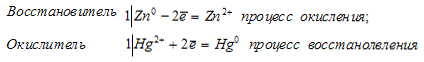
Происходит реакция окисления-восстановления, в которой цинк является восстановителем, а ион ртути Hg2+ - окислитель.
Задача 1027.
Чем объяснить малую диссоциацию хлорида ртути (II) в растворе?
Решение:
В HgСl2 преобладает ковалентная связь, потому что разность электроотрицательностей атомов Hg и Cl (Hg — Cl) равна 1,43 (2.9 – 1,47 = 1,43). Поэтому HgСl2 проявляет свойства как ковалентного соединения, так и ионного. Пары, а также кристаллы HgСl2 состоят из линейных молекул Cl — Hg — Cl, которые практически не диссоциируют в водных растворах.
Задача 1028.
Закончить уравнения реакций:
а) Zn + NaOH →
б) Zn + NaNO3 + NaOH → NH3 +
в) Hg + HNO3 (избыток) →
г) Hg (избыток) + HNO3 →
д) Hg(NO3)2 + H2S →
е) Hg(NO3)2 + KI (избыток) →
Решение:
а) Zn + 2NaOH → Na2ZnO2 + H2↑;
б) 4Zn + NaNO3 +7NaOH →
→ NH3↑+ 4Na2ZnO2 + 2H2O;
в) 3Hg + 8HNO3 (избыток) →
→ 3Hg(NO3)2 + 2NO↑ + 4H2O;
г) 6Hg (избыток) + 8HNO3 →
→ 3Hg(NO3)2 + 2NO↑ + 4H2O;
д) Hg(NO3)2 + H2S → HgS↓ + 2HNO3
е) 2Hg(NO3)2 + 2KI (избыток) →
→ 3Hg(NO3)2 + I2↓ + 2KNO3

