Получение 5%-ного раствора серной кислоты
Задача 401.
Какой объем воды надо прибавить к 100 мл 20%-ного (по массе) раствора H2SO4 (p = 1,14 г/мл), чтобы получить 5%-ный раствор?
Решение:
Масса 100 мл 20%-ного раствора H2SO4 равна 100 . 1,14 = 114 г. В этом растворе содержится 20% H2SO4, т.е. 22,8г (114 . 0,2 = 22,8). По условию задачи эта масса составляет 5% от общей массы разбавленного раствора. Тогда масса полученного раствора может быть рассчитана по уравнению:

где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Тогда
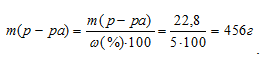
Следовательно, к исходному раствору необходимо прилить 342 г воды (456 – 114 = 342).
Ответ: 342 г.
Задача 402.
К 500 мл 32%-ной (по массе) HNO3 (р = 1,20 г/мл) прибавили 1л воды. Чему равна массовая доля HNO3 в полученном растворе?
Решение:
Массу раствора рассчитаем по формуле: m(р-ра) = pV, где m(р-ра) - масса раствора, p - плотность раствора,
V- объём раствора.
Находим массу раствора HNO3: m(р-ра) - 1,2 . 500 = 600. Находим массу растворённого HNO3:
m(HNO3) = 600 . 0,32 = 192 г.
Масса раствора после смешения составляет 1600 г (600 + 1000 = 1600).
Массовую долю в полученном раствора находим из формулы:

где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Отсюда
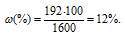
Ответ: 12%.
Задача 403.
До какого объема надо разбавить 500 мл 20%-ного (по массе) раствора NaCl (p = 1,152 г/мл), чтобы получить 4,5%-ный раствор (p = 1,029 г/мл)?
Решение:
Находим массу 500 мл 20%-ного раствора NaCl: m(р-ра) = 115,2 . 500 = 576 г. Масса NaCl, содержащаяся в 576 г этого раствора, составляет 115,2 г (576 . 0,20 = 115,2). Массу раствора NaCl, содержащуюся в растворе с массовой долей 4,5% рассчитаем, используя формулу:содержащуюся в растворе с массовой долей 4,5% рассчитаем, используя формулу:

где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Отсюда

Объём раствора находим по формуле: m(р-ра) = pV, где m(р-ра) - масса раствора, p - плотность раствора,
V - объём раствора.
Отсюда
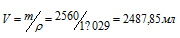 или 2,49л.
или 2,49л.
Ответ: 2,49 л.
Задача 404.
Найти массовую долю азотной кислоты в растворе, в 1 л которого содержится 224 г HNO3 (p = 1,12 г/мл).
Решение:
Находим массу 1 л азотной кислоты по формуле: m(р-ра) = p.V, где m(р-ра) - масса раствора, p - плотность раствора, V - объём раствора.
Отсюда
m(HNO3) = 1,12 . 1000 = 1120 г.
Для расчета массовой доли используем формулу:

где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Отсюда
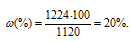
Ответ: 20%.
Задача 405.
Плотность 26%-ного (по массе) раствора КОН равна 1,24 г/мл. Сколько молей КОН находится в 5 л раствора?
Решение:
Находим массу 5л раствора КОН по формуле: m(р-ра) = pV, где m(р-ра) - масса раствора, p - плотность раствора, V - объём раствора.
Отсюда
m(КОН) = 1,24 . 5000 = 6200 г.
Для расчета массы КОН используем формулу:

где
 - массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
- массовая доля растворённого вещества; m(в-ва) - масса растворённого вещества; m(р-ра) - масса раствора.
Отсюда
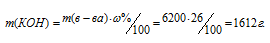
М(КОН)=56 г/моль. Следовательно, количество КОН можно рассчитать:
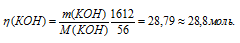
Ответ: 28,8 моль.

