Правильное вычисление потери от растворимости осадка
Задача 211
Вычислить потерю от растворимости осадка в граммах и процентах при промывании его указанным объёмом промывной жидкости. Осадок BaSO4 массой 0,25 г, Пр(BaSO4) =1,1 . 10-10; промывная жидкость Н2SO4, объёмом 500см3, концентрацией 0,02 М.
Решение:
Вычислим растворимость в молях на 1 дм3 BaSO4 в чистой воде, обозначив её через х, получим:
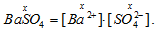
H2SO4 – сильный электролит, и поэтому: 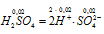 концентрация ионов [SO42-] равна концентрации кислоты: [SO42-] = 0,02 моль/дм3.
концентрация ионов [SO42-] равна концентрации кислоты: [SO42-] = 0,02 моль/дм3.
Так как ионы Ва2+ поступают в раствор только из осадка, то [Ва2+] = х, а ионы из осадка SO42- и из промывной жидкости, тогда [SO42-] = х + 0,02. Поскольку х << 0,02 , то можно считать, что вся концентрация ионов в растворе практически равна его концентрации в промывной жидкости - [SO42-] = 0,02 моль/дм3, а значением х, как очень малой величиной, мы можем пренебречь.
Поскольку Пр(BaSO4) = [Ва2+] . [SO42-], то, подставив в эту формулу соответствующие значения концентраций ионов, находим: Пр(BaSO4) = х . 0,02.
Откуда
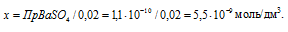
Потери (г) за счёт растворимости равны:
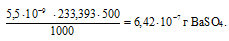
Потери в процентах равны:
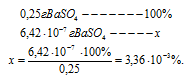
Таким образом, при промывании осадка BaSO4 500 см3, 0,02 М раствора H2SO4 мы вносим очень малую погрешность в результате потерь от растворимости.
Ответ: 6,42 . 10-7г; 3,36 . 10-3.
Задача 212
Вычислить потерю от растворимости осадка в граммах и процентах при промывании его указанным объёмом промывной жидкости. Осадок BaSO4, массой 0,40 г, Пр(BaSO4) =1,1 . 10-10; промывная жидкость Н2SO4, объёмом 300 см3, концентрацией 0,2%.
Решение:
Рассчитаем массу Н2SO4 в 1дм3 раствора из пропорции:
100 : 0,2 = 1000 : х; х = (1000 . 0,2)/100 = 2г Н2SO4.
Рассчитаем концентрацию раствора Н2SO4:
CM(Н2SO4) = m(Н2SO4)/M(Н2SO4) =
= 2/98,066 = 0,0204моль/дм3.
Обозначим растворимость BaSO4 моль/дм3 через х, тогда
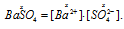
H2SO4 – сильный электролит, и поэтому:
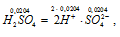
концентрация ионов SO42- равна концентрации кислоты: [SO42-] = = 0,0204 моль/дм3.
Так как ионы Ва2+ поступают в раствор только из осадка, то [Ва2+] = х, а ионы из осадка SO42- и из промывной жидкости, тогда [SO42-] = х + 0,0204. Поскольку х << 0,0204 , то можно считать, что вся концентрация ионов SO42- в растворе практически равна его концентрации в промывной жидкости - [SO42-] = 0,0204 моль/дм3, а значением х, как очень малой величиной, мы можем пренебречь.
Поскольку Пр(BaSO4) = [Ва2+] . [SO42-], то, подставив в эту формулу соответствующие значения концентраций ионов, находим: Пр(BaSO4) = х . 0,0204.
Откуда
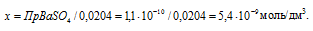
Потери (г) за счёт растворимости равны:
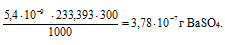
Потери в процентах равны:
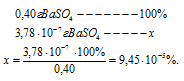
Таким образом, при промывании осадка BaSO4 500 см3 0Б02 М раствора H2SO4 мы вносим очень малую погрешность в результате потерь от растворимости.
Ответ: 3,78 . 10-7г; 9,45 . 10-3%.
Задача 213
Вычислить потерю от растворимости осадка в граммах и процентах при промывании его указанным объёмом промывной жидкости. Осадок BaSO4 массой 0,35г, Пр(BaSO4) = 1,1 . 10-10; промывная жидкость Н2SO4, объёмом 400 см3, концентрацией 1дм3 Н2О + 1 см3, 2 N H2SO4.
Решение:
СМ(H2SO4) = 2СN(H2SO4) = 2/2 = 1M.
Определим концентрацию раствора серной кислоты из пропорции:
1 : 1 = 1000 : х;
х = (1 . 1)/1000 = 0,001M.
Рассчитаем массу Н2SO4 в 1 дм3 раствора из пропорции:
100 : 0,2 = 1000 : х;
х = (1000 . 0,2)/100 = 2г Н2SO4.
Обозначим растворимость BaSO4 моль/дм3 через х, тогда
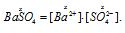
H2SO4 – сильный электролит, и поэтому:
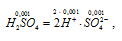
концентрация ионов [SO42-] равна концентрации кислоты: [SO42-] = 0,001моль/дм3.
Так как ионы Ва2+ поступают в раствор только из осадка, то [Ва2+] = х, а ионы из осадка [SO42-] и из промывной жидкости, тогда [SO42-] = х + 0,001. Поскольку х << 0,001 , то можно считать, что вся концентрация ионов [SO42-] в растворе практически равна его концентрации в промывной жидкости - [SO42-] = 0,001моль/дм3, а значением х, как очень малой величиной, мы можем пренебречь.
Поскольку ПрBaSO4 = [Ва2+] . [SO42-], то, подставив в эту формулу соответствующие значения концентраций ионов, находим: Пр(BaSO)4 = х . 0,001.
Откуда
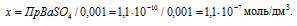
Потери (г) за счёт растворимости равны:
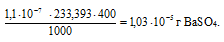
Потери в процентах равны:
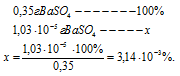
Таким образом, при промывании осадка BaSO4 400 см3 0,001M раствора H2SO4 мы вносим очень малую погрешность в результате потерь от растворимости.
Ответ: 1,03 . 10-5г; 3,14 . 10-3%.
Задачи на вычисление потери от растворимости осадка:
1. Расчет потери от растворимости осадка соли кальция
2. Расчет потери от растворимости осадка карбоната сребра
3. Расчет потери от растворимости осадка хромата свинца

