Заполнение электронных орбиталей атомов элементов | Правила Клечковского
Задача 175.
Сколько значений магнитного квантового числа возможно для электронов энергетического подуровня, орбитальное квантовое число которого l = 2? l = 3?
Решение:
Атомные орбитали, которым отвечает значение орбитального квантового числа l, равное 2, называются d-орбиталями. На d-орбитали (d-подуровне) находится пять АО. Графическая схема d-подуровня имеет вид:
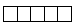
mi - магнитное квантовое число определяет направление электронного облака в пространстве, и принимает значения 0 и целых чисел -1, -2, -3, +1, +2, +3. Так как на d-подуровне содержится пять АО, то, соответственно будет иметь пять разных целочисленных значений, а именно: -2, -1, 0, +1, +2.
Для электронов энергетического подуровня, орбитальное квантовое число которого l = 3, соответствует f-подуровень, содержащий семь АО: . Следовательно, электронам, расположенным на f-подуровне, соответствуют семь значений: -3, -2, -1, 0, +1, +2, +3.
Ответ: 5; 7.
Задача 176.
Какое максимальное число электронов может содержать атом в электронном слое с главным квантовым числом n = 4?
Решение:
В электронном слое с главным квантовым числом n = 4 содержится четыре энергетических подуровня: s-, p-, d- и f-подуровни. Графически это можно представить в виде схемы:
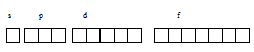
Из схемы вытекает, что в электронном слое с главным квантовым числом n = 4 содержится 16 АО: одна s, три - p, пять - d и семь f. В каждой АО может содержаться по два электрона с противоположными спинами. Таким образом, на четвёртом энергетическом уровне может содержаться 32 электрона (2 . 16 = 32).
Для математического расчёта максимального количества содержания электронов в слое существует простая формула N = 2n2 ,где n - главное квантовое число.
Тогда максимальное число электронов в четвёртом слое равно:
N = 2 . 42 = 32
Ответ: 32.
Задача 177.
Определить по правилу Клечковского последовательность заполнение электронных орбиталей, характеризующихся суммой n + l: а) 5; б) 6; в) 7.
Решение:
Согласно правилам Клечковского, АО заполняются электронами в порядке последовательного увеличения суммы n + l (первое правило Клечковского), и при одинаковых значениях этой суммы – в порядке последовательного возрастания главного квантового числа (2-е правило Клечковского).
а) По условию задачи сумма n + l = 5, причём из всех возможных комбинаций n + l, соответствующих этой сумме (n = 3, l = 2; n = 4, l = 1; n = 5, l = 0), первой будет реализоваться комбинация с наименьшим значением главного квантового числа, т.е. 3d, затем – 4p, а после 4p – 5s.
Таким образом, при сумме n + l =5 порядок заполнения орбиталей будет следующий: 3d?4p?5s..
б) При сумме n + l = 6 из всех возможных комбинаций n + l, соответствующих этой сумме (n + 4, l = 2; n = 5, l = 1; n = 6, l = 0), первой будет реализоваться комбинация с наименьшим значением главного квантового числа, т. е. 4d, затем – 5p, а после 5p – 6s.
Таким образом, при сумме n + l = 6 порядок заполнения орбиталей будет следующий: 4d?5p?6s.
в) При сумме n + l = 7 возможны комбинации n + l, соответствующих этой сумме (n + 4, l = 3; n = 5, l = 2; n = 6, l = 1; n = 7, l = 0), первой будет реализоваться комбинация с наименьшим значением главного квантового числа, т.е. 4f, затем – 5d, далее 6p и уже потом только - 7s.
Таким образом, при сумме n + l = 7 порядок заполнения орбиталей будет следующий: 4f?5d?6p?7s.
Ответ: а) 3d→4p→5s; б) 4d→5p→6s; в) 4f→5d→6p→7s.
Задача 178.
Указать порядковый номер элемента, у которого: а) заканчивается заполнение электронами орбиталей 4d; б) начинается заполнение подуровня 4р.
Решение:
а) 4d-подуровень начинает заполняться после 5s-подуровня. 5s-подуровень начинает заполняться после заполнения электронами 4p-подуровня, т.е. после заполнения оболочки криптона – элемента №36.
Согласно правилу Клечковского после криптона будет заполняться 5s-подуровень, после него – 4d-подуровень. На 5s-подуровне, состоящем из одной атомной орбитали, может находиться два электрона, а на 4d-подуровне, состоящем из пяти атомных орбиталей, может находиться десять электронов. Значит, порядковый номер элемента, с полностью заполненным 4d-подуровнем должен быть на двенадцать больше, чем у криптона (№ 36), значит, элемент № 48 (кадмий). Но, учитывая «провалы» электронов у рутения, родия и палладия с 5s-подуровня на 4d-подуровень (у рутения и родия по одному электрону, а у палладия – два), то 4d-подуровень полностью заполняется электронами у палладия (элемент № 46). Но у элемента № 47 окончательно заканчивается заполнение 4d-орбитали, и 47-й электрон занимает 5s-орбиталь. Таким образом, элемент с порядковым номером 47 считается элементом, у которого заканчивается заполнение электронами 4d-орбитали. Отсюда вывод – порядковый номер элемента 47 (серебро Ag).
б) Согласно правилу Клечковского заполнение электронами 4p-подуровня начинается после заполнения всех атомных орбиталей 3d-подуровня. Элементом, у которого заканчивается заполнение электронами 3d-подуровня является элемент № 30 (цинк). Значит, элементом, у которого начнётся заполнение электронами 4p-подуровня, будет элемент № 31 (галлий Ga).
Ответ: а) Ag; б) Ga.
Задача 179.
Какой подуровень заполняется в атомах после подуровня 5s?
Решение:
Подуровню 5s соответствует сумма n + l, равная 5 (5 + 0 = 5). Такой же суммой n +l характеризуется 4p-подуровень, но заполнению этого подуровня предшествует заполнению 5s-подуровня, так как последнему отвечает большее значение главного квантового числа (второе правило Клечковского). Следовательно, после заполнения 5s-подуровня будет заполняться подуровень с суммой n + l = 6, причём из всех возможных комбинаций n + l, соответствующих этой сумме (n + 4, l = 2; n = 5, l = 1; n = 6, l = 0), первой будет реализоваться комбинация с наименьшим значением главного квантового числа, т.е. вслед за 5s-подуровнем будет заполняться 4d-подуровень n + l = 6.
Ответ: 4d.
Задача 180.
У какого элемента начинает заполняться подуровень 4f? У какого элемента завершается заполнение этого подуровня?
Решение:
Согласно правилам Клечковского 4f-подуровень (n = 4, l = 3) с суммой n + l, равной 7, и с наименьшим значением главного квантового числа, должен заполняться после заполнения 6s-подуровня с суммой n + l, равной 6. Электронную конфигурацию последнего энергетического уровня 6s2 имеет атом элемента № 55 (барий). Затем, у элемента № 57 (лантан), должен начать заполняться 4f-подуровень, но, на самом деле у лантана, расположенного непосредственно после бария появляется не 4f-, а 5d-электрон. Однако уже у следующего за лантаном церия (Z = 58) действительно начинается застройка 4f-подуровня, на который переходит и единственный 5d-электрон, имевшийся в атоме лантана, в соответствии с этим электронная структура атома церия выражается формулой [Kr]4f26s2. Начиная с церия, происходит последовательное заполнение всех орбиталей 4f-подуровня. Далее, начатое заполнение 4f-подуровня у атома церия заканчивается у иттербия (Z = 70).
Ответ: Ce; Yb.
Задача 181.
Какой подуровень заполняется в атомах после заполнения подуровня 5р? После заполнения подуровня 5d?
Решение:
а) Подуровню 5p соответствует сумма n + l = 6 (5 + 1 = 6). Такой же суммой n + l характеризуются подуровни 4d и 6s. Заполнение 4d-подуровня, согласно 2-му правилу Клечковского, предшествует заполнению подуровня 5p. После заполнения электронами подуровня 5p, согласно 2-му правилу Клечковского, начнёт заполняться 6s-подуровень, которому отвечает большее значение главного квантового числа n (n = 6).
б) Подуровню 5d соответствует сумма n + l = 7 (5 + 2 = 7). Такой же суммой n + l характеризуется подуровень 4f, но заполнение этого подуровня предшествует заполнению подуровня 5d, так как последнему отвечает большее значение главного квантового числа. Следовательно, согласно 1-го правила Клечковского, будет заполняться подуровень, которому отвечает на единицу большее значение n + l (n = 6) при сумме n + l = 7. Этому условию отвечает подуровень 6p (n = 6, l = 1) при сумме n + l = 7.
Ответ: 6s; 6p.
Задача 182.
Записать электронные формулы атомов элементов с зарядом ядра: а) 8; б) 13; в) 18; г) 23; д) 53; е) 63; ж) 83. Составить графические схемы заполнения электронами валентных орбиталей этих атомов.
Решение:
Электронные формулы отображают распределение электронов в атоме по энергетическим уровням, подуровням (атомным орбиталям). Электронная конфигурация обозначается группами символов nlx, где n - главное квантовое число, l - орбитальное квантовое число (вместо него указывают соответствующие буквенные обозначения – (s, p, d, f), x – число электронов в данном подуровне (орбитали). При этом следует учитывать, что электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией – меньшая сумма n + l (1-е правило Клечковского), а при одинаковых значениях суммы n + l - в порядке последовательного возрастания главного квантового числа (2-е правило Клечковского). Последовательность заполнения энергетических уровней следующая:
1s →2s → 2p → 3s → 3p→4s → 3d → 4p → 5s → 4d → 5p→ 6s →
→ (5d1) → 4f → 5d → 6p→7s → (6d1-2) → 5f → 6d →7p.
Так как число электронов в атоме элемента численно равно его порядковому номеру в таблице Д.И. Менделеева, то электронные формулы элементов №№ 8, 13, 18, 23, 53, 63, 83 будут иметь вид:
а) +8О 1s22s22p4;
б) +13Al 1s22s22p63s23p1;
в) +18Ar 1s22s22p63s23p6;
г) +23V 1s22s22p63s23p63d34s2;
д) +53I 1s22s22p63s23p63d104s24p64d105s25p5;
е) +63Eu 1s22s22p63s23p63d104s24p64d104f75s25p66s2;
ж) +83Bi 1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p3.
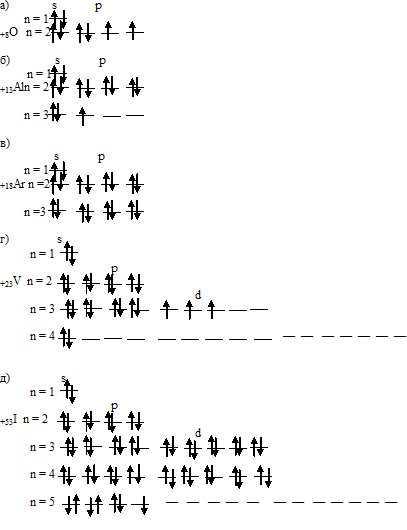
Графические схемы заполнения валентных орбиталей атомов элементов:
Электронная структура атома может быть изображена также в виде схем размещения электронов в квантовых (энергетических) ячейках, которые являются схематическим изображением атомных орбиталей (АО). Квантовую ячейку обозначают в виде прямоугольника  , кружочка
, кружочка  или линейки
или линейки  , а электроны в этих ячейках обозначают стрелками
, а электроны в этих ячейках обозначают стрелками 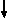 . В каждой квантовой ячейке может быть не более двух электронов с противоположными спинами, например
. В каждой квантовой ячейке может быть не более двух электронов с противоположными спинами, например 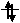
Мы будем применять линейки. Орбитали данного подуровня заполняются сначала по одному электрону с одинаковыми спинами, а затем по второму электрону с противоположными спинами (правило Хунда):