Методы решения расчетных задач по химии, связанные с концентрацией растворов
Во всех задачах этой группы присутствуют расчеты, связанные с концентрацией растворов. Причем во всех тестах используется единственный способ выражения концентрации — массовая доля. Поэтому при решении практически всех задач В9 мы будем пользоваться соотношением для определения массовой доли:
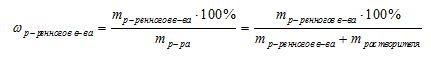
Анализ всех задач, предлагавшихся для решения, за последние годы позволяет распределить их на четыре группы:
1. Определение массы растворенного вещества в определенной порции раствора при известной концентрации;
2. Приготовление раствора путем растворения определенного количества вещества в некотором объеме (массе) растворителя;
3. Изменение концентрации уже имеющегося раствора одним из следующих способов:
а) добавлением к раствору того же растворенного вещества;
б) добавлением к раствору растворителя;
в) смешиванием двух различных растворов одного и того же вещества;
г) выпариванием растворителя или растворенного вещества из раствора.
4. Использование химической реакции в процессе приготовления раствора.
В этой статье,рассмотрим задачи 1-й из вышеперечисленных четырех групп.
Определение массы растворенного вещества в растворе
Задача 1.
Масса соли, которая вводиться в организм при вливании 353 г физиологического раствора, содержащего 0,85% (по массе) поваренной соли, равна ... г (запишите число с точностью до целых).
Дано:
масса раствора: mр-ра = 353 г;
массовая доля растворенного вещества:  в-ва = 0,85% .
в-ва = 0,85% .
Найти: массу растворенной соли.
Решение:
Задача решается в одно действие путем непосредственного проставления данных из условия в соотношение для вычисления массовой доли растворенного вещества.
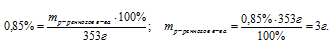
Ответ: масса растворенного вещества равна 3г.
Задача 2.
Какая масса азотной кислоты содержится в 1 л ее 20% раствора с плотностью 1,05 г/мл? Ответ: ... г (запишите число с точностью до целых).
Дано:
объем раствора азотной кислоты: Vр-ра — 1 л;
массовая доля HNO3в р-ре :  (НNO3) = 20%
(НNO3) = 20%
плотность раствора: pр-ра = 1,05 г/мл.
Найти: массу азотной кислоты: m(НNO3) = ?
Решение:
В первую очередь необходимо от объема раствора перейти к его массе, используя плотность. При этом следует учесть, что объем указан в литрах, а плотность в г/мл. Переведем значение
объема в единицы измерения, соответствующие плотности:
Vр-ра = 1л = 1000 мл
mр-ра = Vр-ра . рр-ра = 1000 . 1,05 = 1050г.
Далее используем соотношение для определения массовой доли.
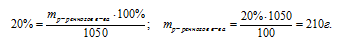
Ответ: m(НNO3) 210 г.
Источник:
ЕГЭ. Химия. Расчетные задачи в тестах ЕГЭ. Части А, В, С / Д.Н. Турчен. — М.: Издательство «Экзамен», 2009. — 399 [1]с. (Серия «ЕГЭ. 100 баллов»). I8ВN 978-5-377-02482-8.

