Количественное осаждение солей хлорида железа (ⅠⅠⅠ) и кристаллогидрата сульфата магния
Уравнения реакции осаждения кристаллогидрата сульфата магния
Задача 119.
Написать уравнения реакции осаждения, рассчитать объём осадителя, необходимый для проведения количественного осаждения, и описать условия осаждения. Исследуемое вещество MgSO4 . 7H2O, навеска массой 0,75 г; осадитель
Na2HPO4 . 12H2O, концентрация 6%.
Решение:
Уравнение реакции осаждения:
3MgSO4 . 7H2O + 2Na2HPO4 . 12H2O =
= Mg3(PO4)2↓ + 2Na2SO4 + Н2SO4 + 19H2O
Так как вещества реагируют в химических реакциях равным числом грамм-эквивалентов, то n1 = n2.
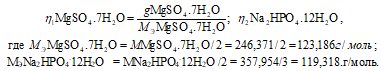
Согласно закону равенства эквивалентов:
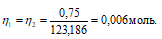
Рассчитаем массу Na2HPO4 . 12H2O:
m(Na2HPO4 . 12H2O) =
= MЭ(Na2HPO4 . 12H2O) . n(Na2HPO4 . 12H2O) =
= (119,318 . 0,006) = 0,73 г.
Теперь рассчитаем объём раствора Na2HPO4 . 12H2O, теоретически необходимый для осаждения 1,20г MgSO4 . 7H2O из пропорции:
100 : 6 = х : 0,73;
х = (0,73 . 100)/6 = 12,16 см3.
Для полного осаждения необходимо брать полуторный избыток раствора осадителя от теоретически расчётного, т.е. объём Na2HPO4 . 12H2O, необходимый для осаждения:
V(Na2HPO4 . 12H2O) = (1,5 . 12,16) = 18,9 см3.
Условия осаждения:
Определение осложняется тем, что Mg3(PO4)2 склонен к образованию очень мелких кристаллов, проходящих через поры фильтра, что затрудняет фильтрование и приводит к потерям. Поэтому в начале осаждения создают условия, обеспечивающие получение крупных кристаллов:
- медленно прибавляют осадитель, что необходимо также и для получения более чистого осадка;
- повышают температуру раствора, что, в свою очередь, также повышает растворимость осадка.
Для обеспечения полноты осаждения в конце процесса добавляют избыток осадителя, фильтрование осадка проводят после охлаждения раствора.
Ответ: V(Na2HPO4 . 12H2O) = 18,9см3.
Уравнения реакции осаждения хлорида железа (ⅠⅠⅠ)
Задача 120.
Написать уравнения реакции осаждения, рассчитать объём осадителя, необходимый для проведения количественного осаждения, и описать условия осаждения. Исследуемое вещество FeCl3, навеска массой 1,00 г; осадитель NH4OH, концентрация 12%.
Решение:
Уравнение реакции осаждения:
FeCl3 + 3NH4OH = Fe(OH)3↓ + 3NH4Cl
Так как вещества реагируют в химических реакциях равным числом грамм-эквивалентов, то n1 = n2.
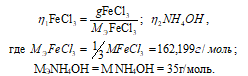
Согласно закону равенства эквивалентов:
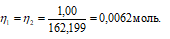
Рассчитаем массу NH4OH:
m(NH4OH) = MЭ(NH4OH) . n(NH4OH) =
= (35 . 0,0062) = 0,215 г.
Теперь рассчитаем объём раствора NH4OH, теоретически необходимый для осаждения 1,00 г FeCl3 из пропорции:
100 : 12 = х : 0,215;
х = (0,215 . 100)/12 = 1,8 см3.
Для полного осаждения необходимо брать полуторный избыток раствора осадителя от теоретически расчётного, т.е. объём NH4OH, необходимый для осаждения:
V(NH4OH) = (1,5 . 1,8) = 2,7 см3.
Условия осаждения:
Определение осложняется тем, что Fe(OH)3 - аморфное соединение, склонено к уплотнению, что затрудняет последующее отмывание осадка, кроме того при стоянни увеличивается количество примесей, адсорбированных развитой поверхностью аморфного осадка. Поэтому Fe(OH)3 отфильтровывают сразу же после осаждения и кратковременного отстаивания.
Необходимые условия осаждения:
Осаждение ведут в присутствии подходящего электролита-коагулятора (обычно это соли аммония), из нагретого анализируемого раствора нагретым раствором осадителя.
- Осаждение ведут из достаточно концентрированного исследуемого раствора концентрированным раствором осадителя.
- Медленно прибавляют осадитель, что необходимо также и для получения более чистого осадка.
- Повышают температуру раствора, что, в свою очередь, также повышает растворимость осадка.
Для обеспечения полноты осаждения в конце процесса добавляют избыток осадителя, фильтрование осадка проводят после охлаждения раствора.
Ответ: V(NH4OH) = 2,7 см3.

