"Химия. 11 класс". О.С. Габриелян (гдз)
Строение атомов. Валентные возможности атомов
Вопрос 1.
Элементы-неметаллы относят к р-элементам, исключением являются Н и Не (s-элементы).
Вопрос 2.
Биогенными элементами являются С, Н, О, S, P, N.
Вопрос 3.
Валентные возможности атомов неметаллов определяются наличием неспаренных электронов и неподелённых электронных пар на внешнем энергетическом уровне.
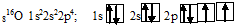
У атома кислорода на внешнем энергетическом уровне содержится 2 неспаренных р-электрона и нет свободных подуровней, поэтому ковалентность кислорода всегда равна двум.
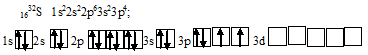
В основном состоянии атом серы содержит на внешнем энергетическом уровне 2 неспаренных 3р-электрона, поэтому сера является двухвалентной.
При возбуждении атома серы электрон с 3р-подуровня может перейти на свободную ячейку 3d-подуровня и, тогда атом будет содержать 4 неспареных электрона, в этом случае сера будет четырёхвалентной:
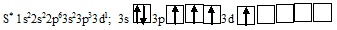
При возбуждении атома серы один электрон с 3р-подуровня, а другой с 3s-подуровня могут перейти на свободные ячейки 3d-подуровня, и тогда атом будет содержать 6 неспареных электронов, в этом случае сера будет шестивалентной:

Вопрос 4.
Разнообразие физических свойств неметаллов объясняется природой вещества.
а) азот, кислород, хлор;
б) бром;
в) иод, сера.
Вопрос 5.
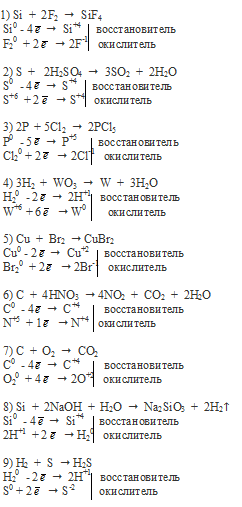
Вопрос 6.
Вода обладает аномально высокой температурой кипения (относительно других халькогеноводородов), что можно объяснить образованием прочных водородных связей между атомами кислорода и водорода, и соседних молекул. При этом образуются комплексы, состоящие из нескольких молекул.
Вопрос 7.
Такое различие свойств можно объяснить увеличением радиуса атомов в группах сверху вниз, а следовательно ослаблением связей Н — Х, поэтому силан на воздухе возгорается, а иодоводород разлагается лишь при небольшом нагревании.
Вопрос 8.
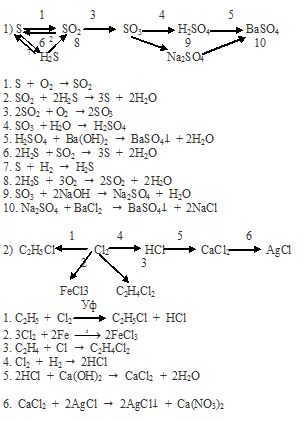
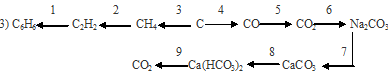
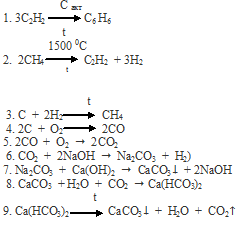
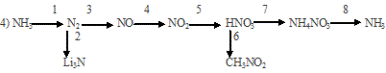
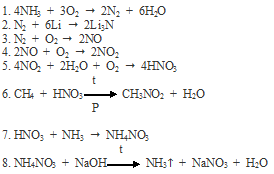
Вопрос 9.
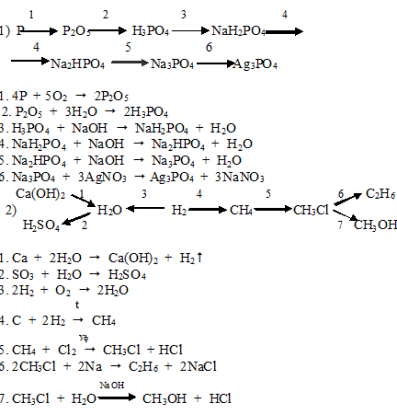
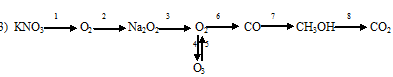
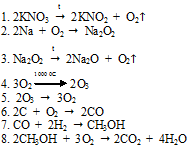

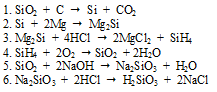
Вопрос 10.
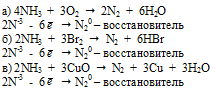
Вопрос 11.
Сходства в свойствах СО2 и SiO2, Н2СО3 и H2SiO3 можно объяснить тем, что С и Si находятся в IV группе главной подгруппы рядом по вертикали. Различия объясняются тем, что радиус атома кремния больше радиуса атома углерода, поэтому он образует немного менее прочные связи, а также соединения кремния проявляют более слабый кислотный характер, чем соответствующие соединения углерода.
Вопрос 12.

Вопрос 13.
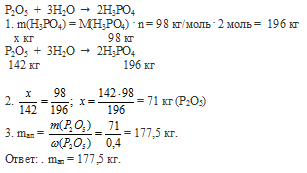
Вопрос 14.
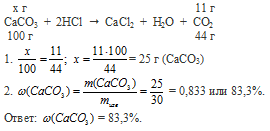
Вопрос 15.
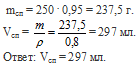
Вопрос 16.
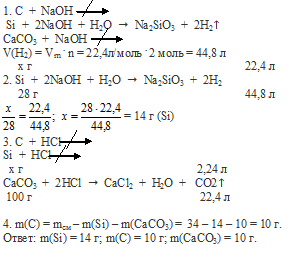
Вопрос 17.

Вопрос 18.

Вопрос 19.
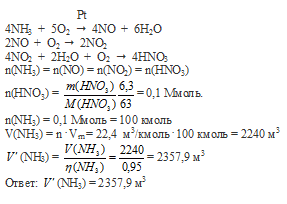
Вопрос 20.
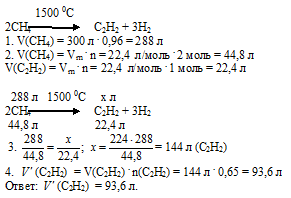
Вопрос 21.
Определение истинной формы алкина


