"Химия. 10 класс". О.С. Габриелян (гдз)
Строение и свойства белков
Вопрос 1.
Белки – природные полимеры, мономерами которых являются аминокислоты (20 природных L – аминокислот). Белковые полимеры – это полипептидные цепи последовательно соединённых аминокислот – первичная структура. Молекула белка обычно содержит неполярные и полярные радикалы. Неполярные радикалы располагаются внутри молекулы, полярные ионогенные группы на поверхности молекулы, полярные неионогенные радикалы могут располагаться как на поверхности, так и внутри белковой молекулы. Все эти радикалы участвуют в закручивании полипептидной цепи при помощи водородных, сульфидных и ионных связей, а также электростатического притяжения - вторичная структура, а также они участвуют в образовании третичной структуры полипептида – сворачивании и изгибании полипептидной цепи. Водородные связи не участвуют в образовании третичной структуры белка.
Вопрос 2.
Пептид – полимер, содержащий небольшое число мономеров – аминокислот. Дипептиды, трипептиды имеют небольшую молярную массу, обычно до 500 г/моль.
Полипептид – полимер, мономерами которого являются аминокислоты, но, в отличие от пептида, содержит большое количество аминокислот. Молярная масса полипептида может достигать величины до 10000 г/моль.
Полиамид – полимер, молярная масса которого может быть 10000-30000 г/моль, мономерами являются аминокислоты.
Белки – полимеры, мономерами которых являются природные аминокислоты. Молярная масса белка обычно больше 30000 г/моль.
Вопрос 3.
Огромное разнообразие природных белков не даёт возможности сформировать их физические свойства. По своим физическим свойствам белки представляют собой твёрдые вещества, растворимые или нерастворимые в воде с различными температурами кипения и плавления.
Химические свойства белков:
1. Гидролиз – образуются аминокислоты.
2. Денатурация – процесс разрушения третичной и вторичной структур белка, который обычно протекает под действием кислот, щелочей, солей тяжёлых металлов при, нагревании, радиации, органических кислот и других факторов.
3. Горение – при сжигании белки обугливаются, и при этом появляется специфический запах жжёного пера (рога).
Вопрос 4.
Качественные реакции на белки:
а) ксантопротеиновая реакция – при действии концентрированной азотной кислоты на раствор белка выпадает ярко-жёлтый осадок.
б) биуретовая реакция – при действии раствора щёлочи в присутствии сульфата меди (II) на раствор белка появляется сине-фиолетовое окрашивание раствора.
Вопрос 5.
В организме человека белки играют важнейшую роль. Они выполняют следующие функции:
а) каталитическую (ферменты);
б) регуляторную (гормоны);
в) запасающую (резервные питательные вещества);
г) защитную (иммуноглобулины, интерфероны);
д) транспортную (гемоглобин);
е) двигательную (лигозин); строительную (коллаген).
Вопрос 6.
Иммунные свойства организмов определяют иммуноглобулин и интерферон.
Вопрос 7.
СПИД – синдром иммунодефицита, распространителем является вирус ВИЧ (вирус иммунодефицита человека), который, проникая в организм человека через кровь, разрушает клетки Т-лимфоцитов, которые обеспечивают сопротивляемость организма к различным заболеваниям, так как вырабатывают антитела. Но, заболев СПИДом, организм человека не способен противостоять многим смертельным заболеваниям, к которым у здорового человека вырабатываются противоядия (антитела). И умирают люди не от СПИДа как такового, а от других заболеваний, вируса Герпеса, саркомы, пневмонии и др.
Так как передаётся ВИЧ через кровь, половой контакт и плаценту, то профилактикой является:
1) использовать презервативы при половом контакте;
2) не вести беспорядочные половые связи;
3) пользоваться одноразовыми шприцами, иглами и т.п.;
4) больная мать не должна рожать детей.
Вопрос 8.
Если поджечь кусочек ткани из натурального волокна, то будет наблюдаться выделение специфического запаха жжёного пера (рога) и образование чёрной золы. Синтетическое волокно не горит, оно только плавится.
Вопрос 9.
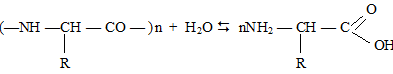
Вопрос 10.