Вычисление массовой доли растворенного вещества
Решение задач по химии на определение массы вещества, молярной массы растворённого вещества
Вычисление массовой доли
Задание 175.
Вычислите массовую долю (%) водного раствора глюкозы С6Н12О6, зная, что этот раствор кипит при 100,26 oС. Эбулиоскопическая константа воды 0,520. Ответ: 8,25%.
Решение:
Температура кипения чистой воды равна 100 oС, следовательно, 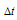 = 100,26 - 100 = 0,260. М( С6Н12О6) = 180 г/моль. Находим массу С6Н12О6 приходящуюся на 1000 г воды используя формулу:
= 100,26 - 100 = 0,260. М( С6Н12О6) = 180 г/моль. Находим массу С6Н12О6 приходящуюся на 1000 г воды используя формулу:
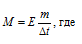
Е – эбулиоскопическая константа; m – масса растворённого вещества; М – молярная масса растворённого вещества; 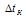 повышение температуры кипения раствора.
повышение температуры кипения раствора.
Отсюда
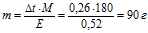
Общая масса раствора, содержащего 90 г глюкозы, составляет 1000 + 90 = 1090 г. Процентное содержание глюкозы в данном растворе находим из соотношения:
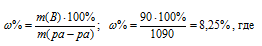
m(B) – масса растворённого вещества m(смеси); m(ра-ра) – масса раствора, которая составляет сумму масс растворителя и растворённого вещества [m(ра-ра) = m(ра-ля) + m(В); - массовая доля растворённого вещества в процентах.
Ответ: 8,25%.
Расчет массы вещества в растворе
Задание 176.
Сколько граммов фенола С6Н5ОН следует растворить в 125 г бензола, чтобы температура кристаллизации раствора была ниже температуры кристаллизации бензола на 1,7°? Криоскопическая константа бензола 5,1°. Ответ: 3,91 г.
Решение:
Для нахождения массы мочевины используем уравнение:
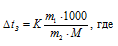
К – криоскопическая константа; m1 – масса растворённого вещества, 5 г; m2 – масса растворителя 95г; М – молярная масса растворённого вещества [М((С6Н5ОН) = 94 г/моль.]; 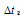 – понижение температуры замерзания раствора.
– понижение температуры замерзания раствора.
Отсюда
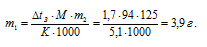
Ответ: 3,9 г.
Задание 177.
Сколько граммов мочевины (NH2)2CO следует растворить в 250 г воды, чтобы температура кипения повысилась на 0,26°? Эбулиоскопическая константа воды 0,52°. Ответ: 7,5 г.
Решение:
Для нахождения массы мочевины используем уравнение:
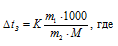
Е – эбулиоскопическая константа; m1 – масса растворённого вещества, 5 г; m2 – масса растворителя 95г; М – молярная масса растворённого вещества [М(NH2)2CO = 60 г/моль]; 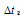 – повышение температуры кипения раствора.
– повышение температуры кипения раствора.
Отсюда
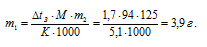
Ответ: 7,5 г
Молярная масса растворенного вещества
Задание 178.
При растворении 2,3 г некоторого неэлектролита в 125 г воды температура кристаллизации понижается на 0,372°. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,86°. Ответ: 92 г/моль.
Решение:
Для расчета используем уравнение:
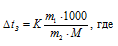
K – криоскопическая константа; m1 – масса растворённого вещества, 2,3 г; m2 – масса растворителя 125г; М – молярная масса растворённого вещества; 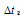 – понижение температуры замерзания раствора.
– понижение температуры замерзания раствора.
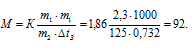
Ответ: 92 г/моль
Вычисление температуры кипения раствора
Задание 179.
Вычислите температуру кипения 15%-ного водного раствора пропилового спирта С3Н7ОН. Эбулиоскопическая константа воды 0,52°. Ответ. 101,625 °С.
Решение:
Рассчитаем повышение температуры кипения пропилового спирта по уравнению, получим::
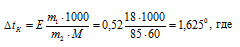
Е – эбулиоскопическая константа; m1 – масса растворённого вещества, 15 г; m2 – масса растворителя 85 (100 -15 = 85) г; М – молярная масса растворённого вещества [М(С3Н7ОН) = 60 г/моль]; 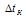 – повышение температуры кипения раствора.
– повышение температуры кипения раствора.
Вода кипит при 100 оС, следовательно, температура кипения раствора равна: 100 - 1,625 = 101,625 оС.
Ответ: 101,625 оС.
Расчет массы метанола в растворе
Задание 180.
Вычислите массовую долю (%) водного раствора метанола СН3ОН, температура кристаллизации которого -2,79 °С. Криоскопическая константа воды 1,86°. Ответ: 4,58%.
Решение:
Температура кристаллизации чистой воды равна 0оС, следовательно, 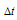 = 0 - (-2,79) = 2,790. М(СН3ОН) = 32 г/моль. Находим массу СН3ОН, приходящуюся на 1000 г воды используя формулу:
= 0 - (-2,79) = 2,790. М(СН3ОН) = 32 г/моль. Находим массу СН3ОН, приходящуюся на 1000 г воды используя формулу:
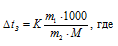
К – криоскопическая константа; m1 – масса растворённого вещества; m2 – масса растворителя; М – молярная масса растворённого вещества; 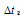 – понижение температуры замерзания раствора.
– понижение температуры замерзания раствора.
Тогда с учётом того, что m2 равно 1000 г, получим:
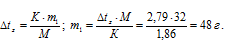
Общая масса раствора, содержащего 48 г метанола, составляет 1000 + 48 = 1048 г. Процентное содержание сахара в данном растворе находим из соотношения:
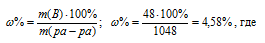
m(B) – масса растворённого вещества m(смеси); m(ра-ра) – масса раствора, которая составляет сумму масс растворителя и растворённого вещества [m(ра-ра) = m(ра-ля) + m(В); - массовая доля растворённого вещества в процентах.
Ответ: 4,58%.

