Реакция внутримолекулярного окисления-восстановления
Реакция термического разложения перманганата калия
Задача 1099.
Написать уравнение реакции термического разложения перманганата калия. К какому типу окислительно-восстановительных превращений относится эта реакция?
Решение:
Уравнение реакции имеет вид:
2КMnO4 = К2MnO4 + MnO2↓ + O2↑.
Здесь марганец уменьшает свою степень окисления в двух случаях от +7 до +6 и от +7 до +4 (является окислителем), а кислород увеличивает сою степень окисления от -2 до 0 (является восстановителем). Реакции, при которых одна составная часть сложного вещества служит окислителем (Mn), а другая – восстановителем (О), называется внутримолекулярной реакцией окисления-восстановления.
Приготовление раствора, содержащего смесь из комбинации ионов
Задача 1100.
Можно ли приготовить раствор, который содержал бы одновременно Sn2+ и Hg2+; Sn2+ и Fe3+; SO32- и MnO4–; Cr2O72- и SO42-? Указать, какие комбинации ионов невозможны и почему.
Решение:
а) В Sn2+ атом элемента находится в своей промежуточной степени окисления, поэтому ион Sn2+ будет проявлять восстановительные свойства. В Hg2+ атом элемента ртути находится в своей высшей степени окисления, поэтому ион Hg2+ будет проявлять только окислительные свойства.
Уравнения полуреакций процесса окисления-восстановления:

Таким образом, приготовить раствор, который содержал бы одновременно Sn2+ и Hg2+ нельзя, так как будет протекать окислительно-восстановительный процесс.
б) В Sn2+ атом элемента находится в своей промежуточной степени окисления, поэтому ион Sn2+ будет проявлять восстановительные свойства. В Fe3+ атом элемента железа находится в своей высшей степени окисления, поэтому ион Fe3+ будет проявлять только окислительные свойства. Уравнения полуреакций процесса окисления-восстановления:
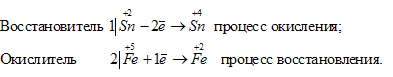
Таким образом, приготовить раствор, который содержал бы одновременно Sn2+ и Fe3+ нельзя, так как будет протекать окислительно-восстановительный процесс.
в) В SO32- атом элемента серы находится в своей промежуточной степени окисления, поэтому ион SO32- будет проявлять восстановительные свойства. В MnO4– атом элемента марганца находится в своей высшей степени окисления, поэтому ион MnO4– будет проявлять только окислительные свойства. Уравнения полуреакций процесса окисления-восстановления:
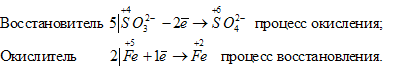
Таким образом, приготовить раствор, который содержал бы одновременно SO32- и MnO4–; нельзя, так как будет протекать окислительно-восстановительный процесс.
г) В Cr2O72- атом элемента хрома находится в своей высшей степени окисления, поэтому ион Cr2O72- будет проявлять окислительные свойства. В SO42- атом элемента серы находится в своей высшей степени окисления, поэтому ион SO42- будет проявлять только окислительные свойства.
Так как в растворе присутствуют ионы Cr2O72- и SO42-, которые оба проявляют окислительные свойства, то приготовит раствор с одновременным содержанием этих ионов возможно.
Ответ: г.

