Типовая задача «В10» на определение объема паров воды
На протяжении нескольких лет во многих вариантах раздела «В10» встречалась следующая задача, требующая некоторых пояснений.
Задача 1.
Объем паров воды, образовавшихся при взаимодействии 3 л Н2 и 2 л О2, равен ... л (запишите число с точностью до целых).
Решение:
На первый взгляд, данная задача ничем не отличается от задачи про горение этана. Но при реакции водорода с кислородом образуется вода:
2Н2 + О2 = 2Н2О.
При условиях проведения реакции, когда выделяется большое количество теплоты и температура довольно высока, вода действительно находится в газообразном состоянии. Но условия (давление и температура), в которых она находится в момент образования, отличаются от условий, при которых измерены объемы исходных веществ. Поэтому для вычисления объема с использованием закона объемных отношений воду необходимо привести к условиям измерения объемов Н2 и О2, а это может послужить причиной ее конденсации.
Решая данную задачу в условиях экзамена, необходимо считать, что исходные объемы Н2 и О2 измерены в таких условиях, в которых вода находится в газообразном состоянии и после реакции всю систему вновь приводят к исходным условиям. Только при таком предположении можно вести расчет по закону объемных отношений.
Применительно к величинам объемов Н2 и О2, указанным в условии, задача решается следующим образом.
1. Определяем, какое из исходных веществ дано в недостатке. Так как и водород, и кислород являются газами, для них применим закон объемных отношений
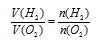
Согласно уравнению реакции
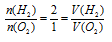
Следовательно, для полного расходования обоих газов объем кислорода должен быть в 2 раза меньше объема водорода.
По условию задачи
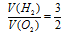
Следовательно, водород дан в недостатке. По нему ведем дальнейший расчет.
2. Считая, что вся вода находится в газообразном состоянии при тех же условиях, что и исходные газы, находим ее объем.
Вновь используем закон объемных отношений:
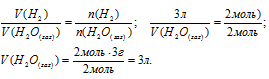
Ответ: V(H2O(газ) = 3л.

