Определение формулы ортофосфата натрия
Задача 3.12.
В 60 г 18% ортофосфорной кислоты растворили 2,84 г оксида фосфора (V) и полученный раствор прокипятили. Какая соль и в каком количестве образуется, если к полученному раствору добавить 30 г гидроксида натрия?
Дано:
масса исходного раствора: mр-ра(Н3РО4) = 60 г;
массовая доля Н3РО4 в исходном р-ре:  (Н3РО4)в исх р-ре = 18% ;
(Н3РО4)в исх р-ре = 18% ;
масса оксида фосфора (V): m(Р2О5) = 2,84 г;
масса гидроксида натрия: m(NаОН) = 30 г.
Найти: формулу образующейся соли и ее количество.
Решение:
При растворении оксида фосфора (V) в водном растворе Н3РО4 при кипячении идет реакция с образованием ортофосфорной кислоты:
Р205 + 3Н2О = 2Н3РО4.
При этом концентрация Н3РО4 в растворе растет.
Далее к полученному более концентрированному раствору Н3РО4 добавляют NаОН. В зависимости от соотношения количеств Н3РО4 и NаОН могут идти реакции с образованием различных типов солей:
3NаОН + Н3РО4 = NаРO4 + 3Н2О;
2NаОН + Н3РO4 = Nа2НРО4 + 2Н2О;
NаОН + Н3РO4 = NаН2РО4 + Н2О.
Причем могут реализоваться следующие ситуации:
а) при большем избытке щелочи [n(NаОН) : n(Н3РО4) > 3 : 1] образуется Nа3РО4 и часть NаОН остается в избытке;
б) при соотношении количеств веществ Н3РО4 и NаОН согласно одному из уравнений образуется только одна из солей.
в) при большом избытке кислоты [n(NаОН) : n(Н3РО4) < 1 : 1] образуется только кислая соль и часть Н3РО4 остается в избытке.
г) когда соотношение количеств вещества Н3РО4 и NаОН находится в промежутке
[1 : 1 < n(NаОН) : n(Н3РО4) < 3 : 1]
и не соответствует ни одной из реакций образуется смесь из двух солей1.
Для того, чтобы определить, какая из четырех возможных ситуаций реализуется в данной задаче необходимо найти соотношение количеств веществ NаОН и Н3РО4.
1. Определим массу Н3РО4 в растворе до растворения в нем Р2O5:
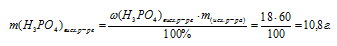
2. Определим массу Н3РО4, которая образуется по реакции из 2,84 г Р2О5:
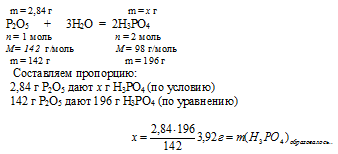
3. Находим общую массу Н3РО4 после растворения Р2О5:
m(Н3РО4)общ =
= m(Н3РО4)в исх р-ре + m(Н3РО4)образовалось =
= 10,8 + 3,92 = 14,72 г.
4. Находим количество вещества Н3РО4.
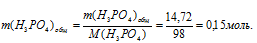
5. Находим количество вещества NаОН:
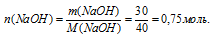
6. NаОН находится в большом избытке по отношению к Н3РО4
nН3РО4: n(Н3РО4) = 0,75 : 0,15 > 3 : 1
Следовательно, образуется средняя соль, и часть NаОН останется в избытке.
Количество вещества образующейся средней соли можно рассчитать по уравнению с образованием средней соли, используя значение количества вещества Н3РО4, т.к. оно в недостатке и расходуется полностью.
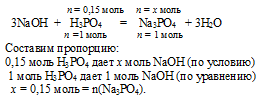
Ответ: m(Nа3РО4) = 0,15 моль.
Задачи на Определение формулы вещества:
1. Определение формулы органического вещества
2. Определение формулы алкана
3. Определение формулы кетона
Kомментарии:
1Данный случай является наиболее сложным. Задача в которой реализуется такая ситуация подробно рассмотрена в главе, посвященной смесям (№ 4.49 раздел 2.3 четвертой главы второй части книги.).

