Задачи, решаемые при помощи расчета по химическому уравнению
Иногда встречаются задачи, при решении которых требуется во 2-м шаге не только схема превращений, но и уравненное уравнение химической реакции в общем виде с индексами и коэффициентами в буквенном виде. По этому уравнению мы будем вести расчет и составлять пропорцию. Второй шаг в таких задачах часто вызывает значительные затруднения как у школьников, так и у абитуриентов.
При уравнивании таких уравнений можно порекомендовать считать буквенные выражения наравне с числовыми и действовать с ними как с обычными числами.
И еще одна полезная рекомендация: после того как вы расставили все коэффициенты (во 2-м шаге), проверьте еще раз равенство атомов каждого элемента. Именно на этом этапе бывает наибольшее количество ошибок во время проверочных работ и на экзаменах.
Примеры решения таких задач.
Задача 96.
При полном сгорании 2,3 моль предельного одноатомного спирта расходовалось 463,68 л газообразного кислорода (н.у.). Определите молекулярную формулу спирта.
Дано: количество вещества спирта: n(СnН2n+1OH) = 2,3 моль; объем кислорода: V(О2) = 463,68 л.
Найти: молекулярную формулу спирта.
Решение:
Шаг 1. В состав предельного одноатомного спирта входит углерод, водород и кислород. Общая формула предельных одноатомных спиртов: СnН2n+1OH. Водород, соединенный с кислородом, выделен в гидроксильную группу для того, чтобы показать принадлежность к классу спиртов. Но для составления уравнения и вывода формулы удобно показать общее число атомов каждого элемента, не различая их по функциональности. Поэтому запишем: СnН2n+2O. Из общей формулы видно, что в 1 молекуле предельного одноатомного спирта содержится один атом кислорода1, а количество атомов водорода строго зависит от количества атомов углерода.
Шаг 2. Составим уравнение реакции горения и уравняем его:
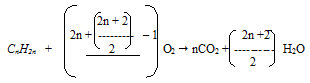
Попытаемся упростить некоторые коэффициенты, пользуясь знаниями из курса алгебры.
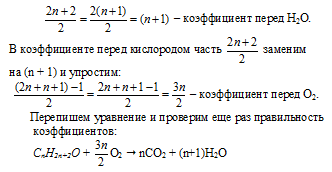
|
Элемент |
Левая часть уравнения |
Правая часть уравнения |
Результат |
| С |
1 . n |
n . 1 | Уравнено |
| Н | 1 . (2n + 2) = 2n + 2 | (n + 1) . 2 = 2n + 2 | Уравнено |
| О | 1 . 1 + (3n/2) . 2 = 1 + 3n | n . 2 + (n +1) . 1= = 2n + n - 1= 3n + 1 |
Уравнено |
Шаг 3. Соотношение атомов однозначно определяется общей формулой:
n(С) : n(Н) : n(О) = 1 : 4 : 1
Шаг 4. Простейшая формула получается из общей формулы предельных одноатомных спиртов: СН4О.
Шаг 5. В этом шаге путем расчета по химическому уравнению мы установим индексы в истинной молекулярной формуле спирта. Для этого по уравнению реакции достаточно составить пропорцию, используя данные из условия. Для расчета по уравнению необходимо по значению объема, указанному в условии, вычислить количество вещества газообразного двухатомного (!) кислорода (н. у.).
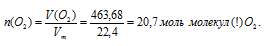
Теперь с помощью уравнения реакции горения составляем пропорцию и определяем «n»:
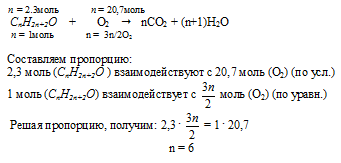
Подставляя это значение в общую формулу, получаем молекулярную формулу искомого спирта: С6Н14О. Для придания записи формулы химического смысла выделим отдельно гидроксильную группу: С6Н13ОН.
Ответ: С6Н13ОН.
Задачи на определение формулы вещества:
!. Определение молекулярной формулы вещества
2. Определение молекулярной формулы алкена
3. Определение формулы оксида
Комментарии:
1 Поэтому спирт и называется одноатомный.

