"Химия. 9 класс". О.С. Габриелян (гдз)
Окислительно-восстановительные свойства металлов. Ряд напряжения металлов
Вопрос 1.
Уравнение реакции образования железной окалины имеет вид:
3Fe + 4H2O = Fe3O4 + 4H2↑(I)
Fe3O4 - представляет собой смесь двух оксидов FeO и Fe2O3. Поэтому уравнение реакции (І) можно условно представить в виде двух уравнений и для каждого составить уравнение электронного баланса.
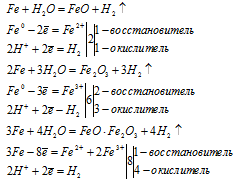
Таким образом, в реакции образования железной окалины три атома железа отдают не 6 и не 9, а 8 электронов.
Вопрос 2.

Вопрос 3.

Вопрос 4.
Щелочные и щелочноземельные металлы очень активны и реагируют практически со всем, с чем соприкасаются. Например, на воздухе эти металлы легко окисляются и, при этом разрушаются. Их хранят под слоем керосина, к которому они инертны, этим они сберегаются от ненужных взаимодействий. Литий — самый легкий из металлов. Он легче керосина и в отличие от других металлов всплывает в нем, поэтому его хранят в вазелине.
Вопрос 5.
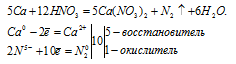
Вопрос 6.
По правилу, которое гласит, что металлы, стоящие в ряду напряжения левее водорода, вытесняют его из растворов кислот, водород при реакции свинца с раствором серной кислоты должен получиться. Но данное правило соблюдается, если в реакции металла с кислотой образуется растворимая соль, а так как PbSO4 — нерастворимая соль то правило не соблюдается, и водород нельзя получить при взаимодействии свинца с раствором серной кислоты.
Вопрос 7.
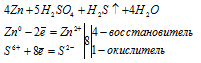
В данной реакции цинк проявляет восстановительные свойства, а сера – окислительные.

