Схемы превращений веществ. Составление уравнений реакций превращений железа
Задание 237.
Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
Fe → FeSO4 → Fe(OH)2 → Fe(OH)3 → FeCl3.
Решение:
Уравнения реакций, которые надо провести для осуществления следующих превращений:
Fe → FeSO4 → Fe(OH)2 → Fe(OH)3 → FeCl3
а) Fe + H2SO4 (разб.) [FeSO4 + H2↑;
б) FeSO4 + 2NaOH → Fe(OH)2↓ + Na2SO4;
в) 4Fe(OH)2↓ + О2 + 2Н2О → 4Fe(OH)3↓;
зелёный буро-красный
осадок осадок
г) Fe(OH)3 + 3HCl → FeCl3 + 3H2O
Задание 429 (ш)
Составьте молекулярные и ионно-молекулярные уравнения реакций, которые надо провести для осуществления превращений:
Fe → FeCl2 → Fe(CN)2 → К4[Fe(CN)6] → К3[Fe(CN)6]
К окислительно-восстановительным реакциям составьте электронные уравнения.
Решение:
Молекулярные и ионно-молекулярные уравнения реакций, которые надо провести для осуществления превращений: Fe → FeCl2 → Fe(CN)2 → К4[Fe(CN)6] → К3[Fe(CN)6]
а) Fe + 2HCl = FeCl2 + H2↑ (молекулярная форма);
Fe + 2H+ = Fe2+ + H20 (ионно-молекулярная форма).
б) FeCl2 + 2KCN = Fe(CN)2↓ + 2KCl (молекулярная форма);
Fe2++ 2CN- = Fe(CN)2↓ (ионно-молекулярная форма).
в) В избытке цианида калия осадок Fe(CN)2 растворяется вследствие образования комплексного соединения К4[Fe(CN)6]:
Fe(CN)2 + 4KCN → К4[Fe(CN)6] (молекулярная форма);
Fe(CN)2 + 4CN- → [Fe(CN)6]4- (ионно-молекулярная форма).
г) При действии хлора или брома на раствор жёлтой кровяной соли анион [Fe(CN)6]4- превращается в анион [Fe(CN)6]3-:
2К4[Fe(CN)6] + Cl2 → 2К3[Fe(CN)6] + 2KCl (молекулярная форма);
2[Fe(CN)6]4- + Cl2→ 2[Fe(CN)6]2- + 2Cl- (ионно-молекулярная форма).
Данная реакция является окислительно-восстановительной, так как атом железа увеличивает свою степень окисления от +2 до +3, т. е. проявляет свойства восстановителя; атомы хлора уменьшают свою степень окисления от 0 до -1, т. е. проявляют свойства окислителя:
Уравнения электронного баланса:
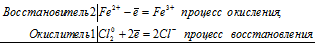
Ионно-молекулярное уравнение:
2Fe2+ + Cl20= Fe3+ + 2Cl-
Молекулярная форма:
2К4[Fe(CN)6] + Cl2 → 2К3[Fe(CN)6] + 2KCl.

