Характеристика аллотропных модификаций фосфора и способы их получения
Задача 911.
Как получают фосфор в промышленности? Написать уравнения соответствующих реакций.
Решение:
Белый фосфор получают при нагревании в электрической печи смеси фосфорита или аппатита, кокса и кварцевого песка. Природный фосфорит или апатит измельчают, смешивают с песком и углем и прокаливают в электрических печах без доступа воздуха. Уравнение реакции можно представить так:
4Са5(РО4)3F +30C + 21SiO2 
 3P4 + 21CaSiO3 + SiF4 + 30CO.
3P4 + 21CaSiO3 + SiF4 + 30CO.
или так:
Ca3(PO4)2 + 3SiO2 + 5C = 3CaSiO3 + 2P + 5CO.
Фосфор выделяется в виде паров, которые конденсируются в приёмнике под водой. Белый фосфор получается в твёрдом состоянии при быстром охлаждении паров фосфора. В результате длительного нагревания белого фосфора без доступа воздуха при атмосферном давлении образуется красный фосфор, а при высоком давлении – кристаллический чёрный фосфор.
Задача 912.
Указать аллотропные модификации фосфора и различия в их свойствах. Сохраняются ли эти различия после перехода фосфора в газообразное состояние? Как доказать, что красный и белый фосфор представляют собой аллотропные модификации одного и того же элемента?
Решение:
Фосфор образует несколько аллотропных модификаций. Важнейшие среди них белый, красный и черный. Белый и красный фосфор термодинамически неустойчивы, но могут существовать при нормальных условиях из-за малых скоростей превращения в устойчивую модификацию — черный фосфор.
Белый фосфор белое мягкое воскообразное вещество или прозрачные кристаллы, состоящие из тетраэдрических молекул Р4 (рис. 1.). Углы Р—Р—Р в таких тетраэдрах равны 60°:
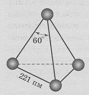
Рис. 1. Структура молекулы
белого фосфора
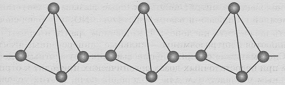
Рис. 2. Структура молекулы красного фосфора
что гораздо меньше 90° между осями р-орбиталей. Эти углы, таким образом, очень напряжены, что придает белому фосфору большую химическую активность. Так как он легко окисляется и может самовоспламеняться на воздухе, его хранят под водой. Белый фосфор ядовит и очень огнеопасен. Молекулярный характер кристаллов придает этой модификации легкоплавкость (tпл. = 44 °С), летучесть (tкип. = 257 °С) и растворимость в органических растворителях.
Красный фосфор существует в нескольких кристаллических формах, которые состоят из связанных между собой бесконечных цепей, образующихся при размыкании тетраэдров (рис. 2.). Он обладает меньшей химической активностью, чем белый, не ядовит, загорается только при поджигании, не растворим в органических растворителях.
Черный фосфор имеет графитоподобную слоистую структуру, в которой каждый атом Р связан с тремя другими (рис. 3.). Слои связаны между собой слабо. Черный фосфор — наименее химически активная аллотропная модификация фосфора.
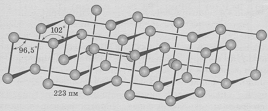
Рис. 3. Структура молекулы чёрного фосфора
Доказательством того, что белый и красный фосфор являются аллотропными модификациями одного и того же элемента служат реакции горения белого и красного фосфора, их активного взаимодействия с с галогенами, с образованием тригалогенидов:
Р4 + 5О2 = Р4О10;
Р4 + 6Cl2 = 4PCl3.
А также то, что при хранении белый фосфор постепенно (очень медленно) переходит в более устойчивую красную форму. Переход сопровождается выделением тепла (теплота перехода):
Р(белый) ⇒ Р(красный) + 4 ккал.

