Задача на определение объема газа, выделившегося при горении этана
Задача 1.
Объем газа (н.у.), который образуется при горении 20,0 л этана (н.у.) в 52,0 л кислорода (н.у.), равен……л. (Запишите число с точностью до десятых).
Дано:
объем этана (н.у.): V(С2Н6) — 20 л;
объем кислорода (н.у.): V(О2) = 52 л.
Найти: объем газа.
Решение:
Записываем реакцию горения этана:
2 С2Н6 + 7О2 → 4СО2 + 6Н2О.
В тестах ЕГЭ в заданиях «В9» и «В10» при горении органических веществ всегда предполагается образование СО2, вне зависимости от количества кислорода или воздуха1.
В задаче требуется определить объем газа. Это требование относится только к СО2, несмотря на то, что в условиях горения образующаяся вода тоже находится в газообразном состоянии. Ее при вычислениях учитывать не надо, т.к. необходимо найти объем газа при нормальных условиях2.
В условии указаны количественные данные, относящиеся к двум исходным веществам одной химической реакции. Это верный признак задачи на избыток-недостаток.
1. Находим количество вещества С2Н6 и О2, принявших участие в первой реакции:
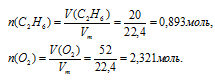
2. Определяем, какое вещество находится в недостатке. Выберем за основу этан и определим по уравнению реакции количество О2, которое необходимо для полного сгорания 0,893 моль С2Н6:
|
n(С2Н6) необходимо |
n(С2Н6) дано по условию |
|---|---|
|
3,126 моль ----> 2,321 моль |
|
О2 находится в недостатке и расходуется весь в процессе реакции. Поэтому дальнейшие расчеты по уравнению реакции будем проводить по кислороду.
3. По уравнению реакции, используя значение количества вещества кислорода, находим объем выделившегося углекислого газа:
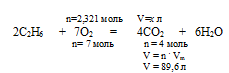
Составляем пропорцию:
2,321 моль О2 дает х л СO2 (по условию)
7 моль О2 дает 89,6 л СО2 (по уравнению)
x =2,321 . 89,6 = 29,7 л = V(CO2).
Ответ: V(CO2) = 29,7 л.
Объем выделившегося углекислого газа можно было найти и по закону объемных отношений, так как и кислород, и СО2 являются газами. Для расчета используем объем кислорода, так как он в недостатке.
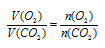
Согласно уравнению реакции 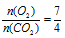 , получим:
, получим:
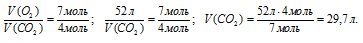
Ответ: V(CO2) = 29,7 л.
Комментарии:
1В реальности при недостатке кислорода может образоваться не только СО2, но и СО. Причем, чем больше молярная масса горящего вещества, тем больше угарного газа образуется при недостатке О2.
2В некоторых задачах, где описана реакция горения органических веществ, нет указания на н.у. Несмотря на это газом надо считать только СО2, не учитывая воду (если нет специальной оговорки по этому поводу).
Задачи на определение объема газа:
1. Определение объема хлора
2. Определение объема водорода
3. Горение метана
Источник:
ЕГЭ. Химия. Расчетные задачи в тестах ЕГЭ. Части А, В, С / Д.Н. Турчен. — М.: Издательство «Экзамен», 2009. — 399 [1]с. (Серия «ЕГЭ. 100 баллов»). I8ВN 978-5-377-02482-8.

