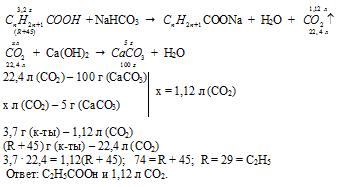"Химия. 10 класс". О.С. Габриелян (гдз)
Строение и свойства карбоновых кислот
Непредельные карбоновые кислоты
Вопрос 1.
Элаидиновая кислота (транс-9-октадеценовая кислота)
Сокращенная структурная формула элаидиновой кислоты:
СН3(СН2)7СН=СН(СН2)7СООН.
Структурная формула элаидиновой кислоты:
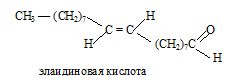
Жирные карбоновы кислоты
Вопрос 2.
В результате реакции гидрирования олеиновой кислоты получается стеариновая кислота:
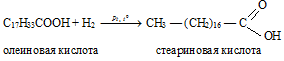
Вопрос 3.
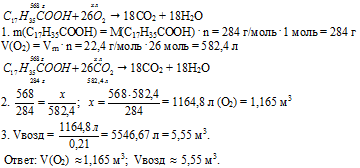
Вопрос 4.
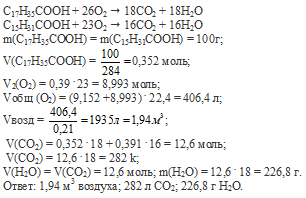
Вопрос 5.

Свойства и применение карбоновых кислот
Вопрос 6.
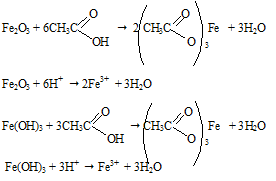
Если обработать раствором кислоты пятно ржавчины, то оно исчезает, так как происходит химическая реакция, ржавчина превращается в растворимый ацетат железа (III), а с водой ни Fe2O3, ни Fe(OH)3 не реагируют, поэтому пятна не удаляются.
Вопрос 7.
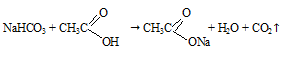
Образование пены можно объяснить бурным выделением пузырьков углекислого газа, выделяющегося при реакции кислоты и соды.
Вопрос 8.
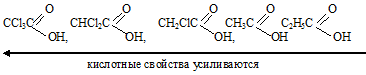
Это можно объяснить строением молекул.
Атомы хлора, как более электроотрицательные, по сравнению с атомами углерода, кислорода и водорода, оттягивают электронную плотность на себя, тем самым не позволяя радикалу компенсировать недостаток электронной плотности на атоме углерода, входящему в состав карбоксильной группы, вследствие чего связь О—Н более полярна.
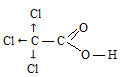
Так как в состав последующих кислот входит меньшее количество атомов хлора, следовательно, связи О—Н в них менее полярны и кислоты с уменьшением количества атомов хлора становятся слабее:

Пропионовая кислота слабее этановой, так как радикал C2H5 — обладает большим +I эффектом, чем СН3 —, т. е. больше отталкивает от себя электронную плотность и связь O—H становится менее полярна по сравнению с таковой в этановой кислоте.
Вопрос 9.
Так как в молекуле муравьиной кислоты отсутствует углеводородный радикал и присутствует альдегидная группа, то она вступает в "реакцию серебряного зеркала":
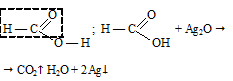
В результате реакции выделяется углекислый газ.
Вопрос 10.
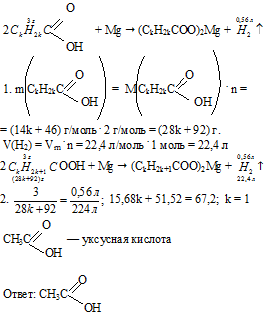
Характерным признаком произошедшей реакции является изменение окраски осадка: был голубой осадок Cu(OH)2, а выпал красный осадок Cu2O.
Вопрос 11.

Вопрос 12.
Даже в отсутствие катализатора акриловая кислота обесцвечивает бромную воду:
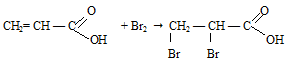
Пропионовая кислота в обычных условиях не реагирует с бромом.
Вопрос 13.
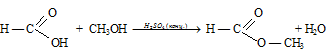
Вопрос 14.
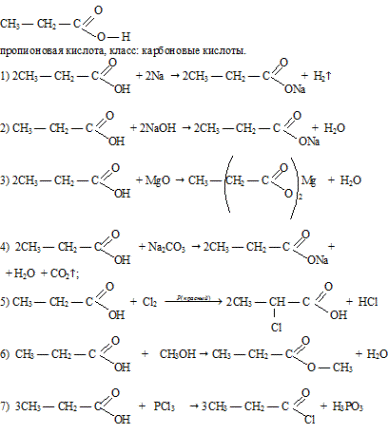
Вопрос 15.
Веществом «А» является:
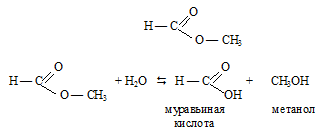
Вопрос 16.
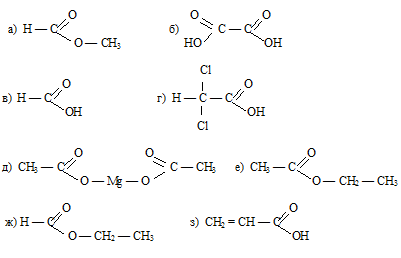
Вопрос 17.
Вопрос 18.