Расчет константы гидролиза, степени гидролиза и рН растворов карбоната натрия
Задача 98.
В 500 см3 раствора содержится Nа2СО3 массой 2,52 г. Определить рН и степень гидролиза соли.
Решение:
V(Nа2СО3) = 500 см3;
m(Nа2СО3) = 2,52 г;
KD1(Н2СО3) = 4,50 · 10–7;
М(Nа2СО3) = 106,00 г/моль;
pH = ?
h = ?
1. Определение молярности раствора соли Nа2СО3
СМ(Nа2СО3) = [m(Nа2СО3) · 1000/500]/М(Nа2СО3) =
= [2,52 · 1000/500]/106,00 = 8,2/82,00 = 0,0475 M.
2. Расчет константы гидролиза соли
Nа2СО3 - соль сильного основания и слабой двухосновной кислоты, поэтому гидролиз, в основном, проходит в одну ступень (1-я ступень) по аниону:
СО32– + H2O = НСО3– + OH–
Константа гидролиза карбоната натрия определяется константой диссоциации по первой ступени образовавшейся кислоты Н2СО3 и определяется по формуле:
Kr = KD(H2O)/KD(кислота)
Тогда
Kr = KD(H2O)/KD1(Н2СО3) =
= (1 · 10-14)/(4,50 · 10–7) = 2,2 · 10–8.
3. Определение степени гидролиза соли
Степень гидролиза определяется по формуле:
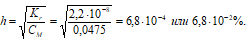
4. Расчет рН раствора соли образованной сильным основанием и слабой кислотой
Так как гидролиз соли Nа2СО3 протекает с выделением ОН- - ионов, то рассчитаем [OH-]:
[OH¯] = h · CM = (6,8 · 10–4)·(0,0475) =
3,2 · 10–5 моль/дм3;
рОН = -lg[OH–] = -lg3,2 · 10–5 = 5 - 0,50 = 4,50;
pH = 14 - pOH = 14 - 4,50 = 9,50.
Ответ: рН = 9,50; h = 6,8 · 10–2%.
Задача 99.
Вычислите рН и степень гидролиза соли в 0,05 М растворе Nа2СО3. Чему будет равен рН, если раствор разбавить водой в 5 раз?
Решение:
KD(Н2О) = 1,00 · 10–14
KD1(Н2СО3) = 4,50 · 10–7;
СМ1(Nа2СО3) = 0,05 М;
pH1 = ?
h1 = ?
pH2 = ?
h2 = ?
а) Вычисление рН и степени гидролиза соли Nа2СО3 до разбавления ее водой
1. Расчет константы гидролиза соли
Nа2СО3 - соль сильного основания и слабой двухосновной кислоты, поэтому гидролиз, в основном, проходит в одну ступень (1-я ступень) по аниону:
СО32– + H2O = НСО3– + OH–
Константа гидролиза определяется константой диссоциации по первой ступени образовавшейся кислоты Н2СО3 и определяется по формуле:
Kr = KD(H2O)/KD(кислота)
Тогда
Kr = KD(H2O)/KD1(Н2СО3) =
= (1 · 10¯14)/(4,50 · 10–7) = 2,2 · 10–8.
2. Определение степени гидролиза соли до разбавления ее водой
Степень гидролиза определяется по формуле:
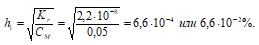
3. Расчет рН1 раствора соли Nа2СО3 до разбавления
Так как гидролиз соли Nа2СО3 протекает с выделением ОН– - ионов, то рассчитаем [OH–]:
[OH–]1 = h · CM = (6,6 · 10–4)·(0,05) =
= 3,32 · 10–5 моль/дм3;
рОН1 = -lg[OH–]1 = -lg3,32 · 10–5 = 5 - 0,52 = 4,48;
pH1 = 14 - pOH = 14 - 4,50 = 9,50.
б) Вычисление рН и степени гидролиза соли Nа2СО3 после разбавления ее водой
Так как раствор соли разбавили водой в 5 раз, то и молярность раствора уменьшилась тоже в 5 раз
Тогда
СМ2(Nа2СО3) = СМ1(Nа2СО3)/5 = 0,05/5 = 0,01 M.
1. Определение степени гидролиза соли после разбавления ее водой
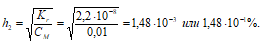
2. Расчет рН2 раствора соли Nа2СО3 после разбавления ее водой
Так как гидролиз соли Nа2СО3 протекает с выделением ОН– - ионов, то рассчитаем [OH–]:
[OH–]2 = h · CM = (1,48 · 10–3)·(0,01) =
= 1,48 · 10–5 моль/дм3;
рОН2 = -lg[OH–]2 = -lg1,48 · 10–5 = 5 - 0,17 = 4,83;
pH2 = 14 - pOH = 14 - 4,83 = 9,17.
Ответ: рН1 = 9,52; h1 = 0,066%; h2 = 0,148%; рН2 = 9,17.
Задача 100.
Вычислите рН и степень гидролиза соли в 0,05 М растворе Nа2СО3. Чему будет равен рН, если раствор разбавить водой в 10 раз?
Решение:
KD(Н2О) = 1,00 · 10–14;
KD1(Н2СО3) = 4,50 · 10–7;
СМ1(Nа2СО3) = 0,05 М;
pH1 = ?
h1 = ?
pH2 = ?
h2 = ?
а) Вычисление рН и степени гидролиза соли Nа2СО3 до разбавления ее водой
1. Расчет константы гидролиза соли
Nа2СО3 - соль сильного основания и слабой двухосновной кислоты, поэтому гидролиз, в основном, проходит в одну ступень (1-я ступень) по аниону:
СО32– + H2O = НСО3– + OH–
Константа гидролиза определяется константой диссоциации по первой ступени образовавшейся кислоты Н2СО3 и определяется по формуле:
Kr = KD(H2O)/KD(кислота)
Тогда
Kr = KD(H2O)/KD1(Н2СО3) = (1 · 10–14)/(4,50 · 10–7) = 2,2 · 10–8.
2. Определение степени гидролиза соли до разбавления ее водой
Степень гидролиза определяется по формуле:
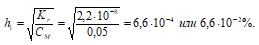
3. Расчет рН1 раствора соли Nа2СО3 до разбавления
Так как гидролиз соли Nа2СО3 протекает с выделением ОН– - ионов, то рассчитаем [OH–]:
[OH–]1 = h · CM = (6,6 · 10–4)·(0,05) = 3,3 · 10–5 моль/дм3;
рОН1 = -lg[OH–]1 = -lg3,3 · 10–5 = 5 - 0,52 = 4,48;
pH1 = 14 - pOH = 14 - 4,48 = 9,52.
б) Вычисление рН и степени гидролиза соли Nа2СО3 после разбавления ее водой
Так как раствор соли разбавили водой в 10 раз, то и молярность раствора уменьшилась тоже в 10 раз
Тогда
СМ2(Nа2СО3) = СМ1(Nа2СО3)/5 = 0,05/10 = 0,005 M.
1. Определение степени гидролиза соли после разбавления ее водой
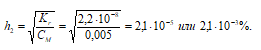
2. Расчет рН2 раствора соли Nа2СО3 после разбавления ее водой
Так как гидролиз соли Nа2СО3 протекает с выделением ОН– - ионов, то рассчитаем [OH–]:
[OH–]2 = h · CM = (2,1 · 10–5)·(0,005) = 1,05 · 10–7 моль/дм3;
рОН2 = -lg[OH–]2 = -lg1,05 · 10–7 = 7 - 0,02 = 6,98;
pH2 = 14 - pOH = 14 - 6,98 = 7,02.
Ответ: рН1 = 9,52; h1 = 0,066%; h2 = 1,05 · 10–3%; рН2 = 7,02.

