"Химия. 8 класс". О.С. Габриелян (гдз)
Роль Лавуазье в развитии химии
Ответ на вопрос 1 (1).
Лавуазье доказал, что горение — процесс соединения веществ с кислородом, а не как считалось раньше, что это разложение горючих веществ с выделением флогистона — носителя горючести тел.
Основной вклад А. Лавуазье в химию в том, что он заложил основы анализа органических соединений и создал предпосылки для возникновения органической химии.
Ответ на вопрос 2 (2).
Сущность процесса горения в окислении веществ, в результате получаются оксиды элементов, образовавших данное вещество.
Сущность процесса дыхания в поглощении организмом кислорода и выделении углекислого газа.
Сходство этих процессов: в обоих случаях происходит окисление веществ кислородом, но в случае горения это могут быть любые вещества, кроме уже окисленных, (нужно только создать необходимые условия), а в случае дыхания окисляется глюкоза, образуются только СО2 и Н2О.
Современные представления о процессе горения отличаются от представлений Лавуазье в том, что вещества при этом не соединяются с кислородом, а реагируют, окисляясь.
Ответ на вопрос 3 (3).
В доказательство того, что вода сложное вещество, приводят электролиз воды, в результате которого образуются два простых вещества:
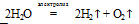
Проверяли это следующим образом: вносили тлеющую лучину в кислород — она вспыхивала, вносили горящую лучину в водород — раздавался хлопок.
Ответ на вопрос 4 (4).
«Элемент» Лавуазье — современный атом, поэтому можно утверждать, что закон сохранения массы соблюдается, так как все атомы, вступающие в реакцию, образуют продукты реакции и больше ни на что не расходуются.
Ответ на вопрос 5 (5).
Потому что не могли доказать, что кремнезем и известь есть сложные вещества, пользуясь лишь существующими тогда методами анализа.
Ответ на вопрос 6 (6).
Современные химики выделили 6 основных классов веществ:
1. Неметаллы
2. Металлы
3. Оксиды: СuО — оксид меди (II), СаО — оксид кальция, Na2O — оксид натрия, Аl2O3 — оксид алюминия, Р2O5 — оксид фосфора (V), СО2 — оксид углерода (IV), N2O — оксид азота (I), SО3 — оксвд серы (VI).
4. Соли: А12(SO4)3 — сульфат алюминия, КСI — хлорид калия, ВаВг2 — бромид бария, Na2SO3 — сульфит натрия, Na2S — сульфид натрия, Рb(NO3)2 — нитрат свинца (II).
5. Кислоты: Н2SO4 — серная кислота, Н2SO3 — сернистая кислота, HNO3 — азотная кислота, HNO2 — азотистая кислота, Н2SiO3 — кремниевая кислота, Н2S — сероводородная кислота, НСI — хлорoводородная кислота, Н3PO4 — фосфорная кислота.
6. Основания: Са(ОН)2 — гидроксид кальция; Fе(ОН)3 — гидроксид железа (III); NH4OH — гидроксид аммония; КОН — гидроксид калия; Сu(ОН)2 — гидроксид меди (II) (Определения см. § 42, ответ на вопрос 5.).

