Расчеты по термохимическим уравнениям реакций
Задача 1.5.
При сгорании 8,96 л (н.у.) бутана согласно термохимическому уравнению:
2С4Н10 + 13О2 = 8СО2 + 10Н2О + 5757 кДж выделилось:
1) 1151,4 кДж; 2) 2302,8кДж; 3) 4605,6 кДж; 4) 575,7кДж.
Дано: объем ацетилена: V(С4Н10) = 8,96 л.
Найти: количество выделившейся теплоты.
Р е ш е н и е:
Для выбора верного ответа удобнее всего провести расчет искомой в задаче величины и сравнить ее с предлагаемыми вариантами. Расчет по термохимическому уравнению ничем не отличается от расчета по обычному уравнению реакции. Над реакцией мы указываем данные в условии и искомые величины, под реакцией — их соотношения согласно коэффициентам. Теплота представляет собой один из продуктов, поэтому ее числовое значение мы рассматриваем как коэффициент.
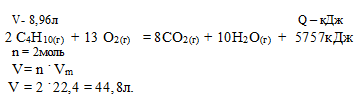
Составляем пропорцию:
8,96 л бутана дают х кДж (по условию)
44,8 л бутана дают 5757 кДж (по уравнению)
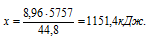
Сравнивая полученный ответ с предложенными вариантами, видим, что подходит ответ № 1.
Ответ: № 1.
Задача 1.6
При полном сгорании некоторого количества бутена выделилось 541,4 кДж. При этом согласно термохимическому уравнению:
2С4Н8 + 12О2 = 8СО2 + 8Н2О + 5414 кДж объем образовавшегося СО2 (н.у.) составил:
1) 4,48 л; 2) 8,96 л; .3) 17,92 л; 4) 22,4 л.
Дано: Количество выделившейся теплоты: Q = 541,4 кДж.
Найти: объем углекислого газа (н.у.): V (CO2) = ?
Р е ш е н и е :
Для выбора верного ответа удобнее всего провести расчет искомой в задаче величины и сравнить ее с предлагаемыми вариантами. Расчет по термохимическому уравнению ничем не отличается от расчета по обычному уравнению реакции. Над реакцией мы указываем данные в условии и искомые величины, под реакцией — их соотношения согласно коэффициентам. Теплота представляет собой один из продуктов, поэтому ее числовое значение мы рассматриваем как коэффициент.
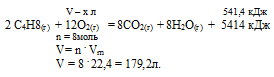
Для вычисления объема углекислого газа составляем пропорцию:
х л бутена дают 444 кДж (по условию)
179,2 л бутана дают 5414 кДж (по уравнению)
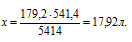
Сравнивая полученный ответ с предложенными вариантами, видим, что подходит ответ № 3.
Ответ: V(CO2) = 17,92 л.
Задача 1.7
При сгорании порции пропана выделилось 444 кДж теплоты. Согласно термохимическому уравнению: С3Н8 + 502 = ЗСО2 + 4Н2О + 2220 кДж, объем (н.у.) затраченного кислорода равен:
1)44,8 л; 2) 17,92 л; 3) 22,4 л; 4) 11,2 л.
Дано: Количество выделившейся теплоты: Q = 444 кДж.
Найти: объем углекислого газа (н.у.): V (O2) = ?
Р е ш е н и е :
Для выбора верного ответа удобнее всего провести расчет искомой в задаче величины и сравнить ее с предлагаемыми вариантами. Расчет по термохимическому уравнению ничем не отличается от расчета по обычному уравнению реакции. Над реакцией мы указываем данные в условии и искомые величины, под реакцией — их соотношения согласно коэффициентам. Теплота представляет собой один из продуктов, поэтому ее числовое значение мы рассматриваем как коэффициент.
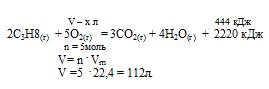
Для вычисления объема углекислого газа составляем пропорцию:
х моль кислорода требуется для получения 444 кДж (по условию)
5 моль кислорода требуется для получения 2220 кДж (по уравнению)
Получим:
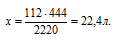
Сравнивая полученный ответ с предложенными вариантами, видим, что подходит ответ № 3.
Ответ: V(O2) = 22,4 л.
Задачи на термохимические уравнения:
1. Термохимические процессы
2. Изменения энергии Гиббса
3. Энергетика химических реакций

