Как правильно рассчитать рН растворов сильных и слабых электролитов
Задача 40.
Вычислите рН 0,025 М раствора КОН.
Решение:
КОН – сильный электролит, который диссциирует по схеме: КОН = К+ + ОН–;
[ОН–] = СМ(КОН) = 0,025 моль/дм3;
рОН = – lg[OH–] = – lg2,5 · 10–2 = 2 – lg2,5 = 2 - 0,6 = 1,4;
pOH + pH = 14;
pH = 14 – pOH = 14 – 1,4 = 12,6.
Ответ: рН = 12,6.
Задача 41.
Вычислите концентрацию ионов [H+] и рН 0,3 М раствора пропионовой кислоты С2Н5СООН, если КD = 1,4 · 10–5.
Решение:
С2Н5СООН – слабая кислота. Для слабых кислот [H+] вычисляется по формуле:
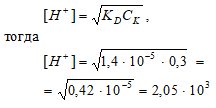
рН = –lg[H+] = –lg2,05 · 10–3 = 3 – lg2,605 = 2,7.
Ответ: [H+] = 2,05 · 10–3 моль/л; рН = 2,7.
Задача 42.
Вычислите рН 0,02 М раствора аммиака, если КD = 1,76·10–5.
Решение:
В водном растворе аммиака имеет место равновесие:
NH3 + H2O ⇔ NН4+ + OH–.
Поскольку КО < 1 · 10–2, полагаем, что равновесная концентрация недиссоциированного основания равна его общей концентрации:
CО(NH4OH) = 0,02 моль/дм3.
Для слабых оснований [H+] вычисляют по формуле:
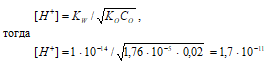
рН = –lg[H+] = –lg1,7 · 10–11 = 11 – lg1,7 = 10,77.
Ответ: [H+] = 1,7 · 10–11 моль/дм3; рН = 10,77.
Задача 43.
К 80 см3 0,2 Н. раствора СН3СООН прибавили 20 см3 0,2 н. раствора СН3СООNa. Рассчитайте рН полученного раствора, если Кк = 1,78 · 10–5.
Решение:
Объём раствора, полученного после сливания исходных растворов, равен 80 + 20 = 100 см3.
Рассчитаем нормальность веществ в полученном растворе смеси, получим:
Сн(СН3СООН) = [Сн(СН3СООН) . V(СН3СООН)]/V(p-pa) =
= (0,2 . 80)/100 = 0,16 моль/дм3;
Сн(СН3СООNa) = [Сн(СН3СООNa) . V(СН3СООNa)]/V(p-pa) =
= (0,2 . 20)/100 = 0,04 моль/дм3.
Для буферных растворов, образованных слабой кислотой и солью этой кислоты, [Н+] находят по формуле:
[H+] = Кк . (Ск/Cc);
Тогда
[H+] = 1,78 · 10–5 . (0,16/0,04) = 7,12 · 10–5 моль/дм3.
рН = –lg[H+]; pH = –lg7,12 · 10–5 = 5 – lg7,12 = 4,15.
Ответ: [H+] = 7,12 · 10–5 моль/дм3; рН = 4,15.
Задача 44.
Вычислите и сравните рН растворов: а) 0,1 М HCl и 0,1 М CH3COOH; б) растворов, содержащих 7 г/дм3 HCl и 7 г/дм3 CH3COOH.
Решение:
а) Расчет рН растворов: 0,1 М HCl, 0,1 М CH3COOH
1. рассчитаем рН раствора 0,1 М HCl
HCl - сильная кислота, которая диссциирует полностью, поэтому
[H+] = СМ(HCl) = 0,1 моль/дм3.
Тогда
рН = –lg[H+]; pH = –lg1 · 10–1 = 1 – lg1 = 1.
2. рассчитаем рН раствора 0,1 М CH3COOH
CH3COOH (Кк = 1,78 · 10–5) – слабая кислота. Для слабых кислот [H+] вычисляется по формуле:
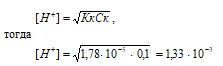
рН = –lg[H+] = –lg1,33 · 10–3 = 3 – lg1,33 = 2,88.
б) Расчет рН растворов, содержащих 7 г/дм3 HCl и 7 г/дм3 CH3COOH
1. Рассчитаем рН раствора HCl
Определим концентрацию HCl, получим:
СМ(HCl) = m(HCl)/M(HCl) = 7/36,5 = 0,19 = 1,9 · 10–1
Так как HCl сильный электролит, то [H+] = См(HCl) = 0,19 = 1,9 · 10–1 моль/дм3.
рН = –lg[H+]; pH = –lg1,9 · 10–1 = 1 – lg1,9 = 0,72.
2. Рассчитаем рН раствора CH3COOH
Определим концентрацию CH3COOH, получим:
СМ(CH3COOH) = m(CH3COOH)/M(CH3COOH) =
= 7/60 = 0,117.
CH3COOH – слабая кислота. Для слабых кислот [H+] вычисляется по формуле:
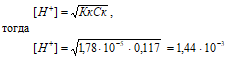
рН = –lg[H+]; pH = –lg1,44 · 10–3 = 3 – lg1,44 = 2,85.
Ответ: а) 1 и 2,88; б) 0,72 и 2,85.

