Расчет молярной массы эквивалента, молярной и относительной атомной массы металла
Задание 10.
Чему равен при н.у. эквивалентный объем кислорода? На сжигание 1,5 г двухвалентного металла требуется 0,69 л кислорода (н.у.) Вычислите молярную массу эквивалента, молярную массу и относительную атомную массу этого металла.
Решение:
Эквивалентный объём кислорода VЭ(О2) равен 22,4/4 = 5,6 л, потому что молекула его состоит из двух двухвалентных атомов кислорода. Согласно закону эквивалентов массы (объёмы) реагирующих веществ m1 и m2 пропорциональны их молярным массам (объёмам):
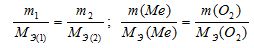
Если одно из веществ находится в газообразном состоянии, то, как правило, его количество измеряется в объёмных единицах (см3, л, м3). Заменив отношение m(O2)/МЭ(О2) равным ему:
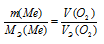
Из этого уравнения находим молярную массу эквивалента металла:
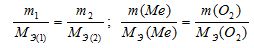
Молярная масса металла определяется из соотношения МЭ = А/В, где МЭ – молярная масса эквивалента металла; А – молярная масса металла; В – стехиометрическая валентность элемента.
Тогда
А = МЭ . В = 12,17 . 2 = 24,34 г/моль.
Так как относительная атомная масса в а. е. м. численно равна относительной молярной массе, выраженной в г/моль, то искомая масса металла равна 24,34 а. е. м.
Ответ: МЭ(МеО) = 12,17 г/моль; МЭ(Ме) = 24,34 г/моль; М(Ме) = 24,34 г/моль; Ar(Ме) = 24,34.

