"Химия. 8 класс". О.С. Габриелян (гдз)
Электролиты. Диссоциация электролитов
Ответ на вопрос 1(1).
а)
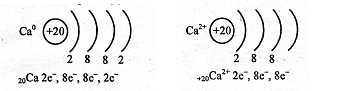
Ca — металл серебристо-белого цвета, реагирует с водой энергично, при этом выделяется Н2 и образуется Са(ОН)2; Са2+ — бесцветные ионы, при реакции с водой ни щелочи, ни водорода не образуют.
б) Cu2+гидр. и Cu2+негидр. имеют одинаковое электронное строение, однако ионы Cu2+гидр. окружены диполями1 воды:
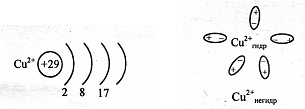
Cu2+гидр. – ионы голубого цвета, Cu2+негидр. – бесцветные ионы.
в) H2 и H+.
Электронное строение: +1H0 1s2; +1H+ 1s0
H2 — бесцветный газ, не имеет запаха, сильный восстановитель при повышенных температурах.
H+ — бесцветные ионы, существуют только в растворе, восстановительными свойствами не обладают.
Ответ на вопрос 2(2).
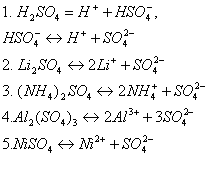
Ответ на вопрос 3(3).

Ответ на вопрос 4(4).
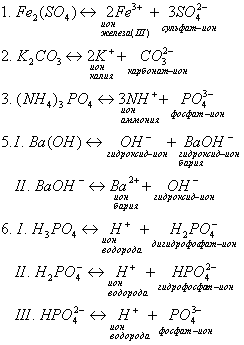
Диссоциация фосфорной кислоты по третьей ступени не происходит.
Ответ на вопрос 5(5).
Диссоциировать будут только растворимые в воде вещества (соли, кислоты, основания), остальные соединения не являются электролитами:
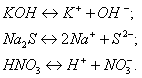
Ответ на вопрос 6(6).
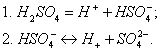
В записи уравнения диссоциации по второй ступени ставится знак обратимости, т.к. по второй ступени диссоциация происходит намного слабее и равновесие сдвинуто влево.
Комментарии:
1Диполь - это молекула с разделенным электрическим зарядом. Например в молекуле воды (Н-О-Н), где водород в силу меньшей электроотрицательности несет положительный заряд, а кислород отрицательный. Та часть молекулы, где кислород, имеет частичный отрицательный заряд, а та часть, где два атома водорода - частично положительный. Происходит это потому, что химические связи О-Н полярные, то есть электроны смещены в сторону атома кислорода. У молекулы воды дипольный момент (в дебаях) 1,84.

